| О журнале | Редколлегия | Редсовет | Архив номеров | Поиск | Авторам | Рецензентам | English |
Зависимость от никотина: диагностика и лечение
Аннотация В статье представлены диагностические критерии МКБ-10 основных патологических состояний, связанных с употреблением никотина. Рассмотрены медико-социальные последствия табакокурения через трубки и кальяны, вред пассивного курения, использования электронных сигарет и некурительных видов табака. Представлены основные инструменты для диагностики степени синдрома зависимости, готовности к отказу от курения и современные средства лечения. Ключевые слова Табачная зависимость, табакокурение, никотиновая зависимость, электронные сигареты, пассивное курение, никотинзаместительная терапия, тест Фагерстрема Введение Федеральный закон от 23 февраля 2013 года № 15-ФЗ "Об охране здоровья граждан от воздействия окружающего табачного дыма и последствий потребления табака", принятый в соответствии с подписанной Рамочной конвенцией ВОЗ по борьбе против табака, вводит ограничения мест курения, торговли табачными изделиями, запрет рекламы и прочие меры, направленные на снижение спроса на табачные изделия, на лечение табачной зависимости и последствий курения табака [16]. По данным ВЦИОМ (опрос проведен в мае 2016 года) за время действия Закона количество курильщиков снизилось с 41% в 2013 году до 31% на момент проведения опроса [2]. При этом до данным ФОМ от 24-25.10.15 только 13% опрошенных хотят бросить курить, но не могут и 9% курильщиков обращались за медицинской помощью по поводу одышки, кашля и отхождения мокроты [18]. Низкая обращаемость за медицинской помощью по поводу табакокурения и неготовность медицинских работников дать необходимую информацию по вопросам лечения зависимости от никотина и последствий курения табака является следствием отсутствия единых требований к организации медицинской помощи и обучения врачей различных специальностей по данной теме. Никотин – основной алкалоид листьев табака, его содержание в сигаретах составляет примерно 95% от всех алкалоидов, содержащихся в этом растении, которых насчитывается более десятка. Он является основным индуктором табачной зависимости. Табачные изделия отличаются по содержанию никотина. В трубочном табаке его примерно столько же, как в обычных сигаретах, а в сигарах и жевательном табаке никотина содержится меньше. Вред, наносимый организму табакокурением, в большей степени связан с вдыхаемым сигаретным дымом, который содержит различные химические вещества, токсичные продукты горения, негативно влияющие на сердечно-сосудистую, дыхательную, иммунную системы. В табачном дыме выявлено более 4000 химических веществ, из них, около 250 опасны для здоровья и более 50 могут стать причиной рака [3]. Острая интоксикация, вызванная употреблением табака (F17.0) Поглощение никотина через мембраны клеток зависит от рН дыма, обычно он имеет кислую реакцию (рН 5,3). Поэтому ионизированный никотин плохо проникает через клеточные мембраны, так как, чем выше значение рН, тем активнее он всасывается. При вдыхании табачного дыма высокая скорость абсорбции никотина объясняется большой площадью поверхности альвеол и значением рН жидкости в легких (pH 7,4), поэтому никотин достигает головного мозга уже через 10-20 секунд после затяжки [25]. Неионизированный никотин (pH 8,5) из дыма трубочного табака и сигар имеет щелочную реакцию и быстро всасывается в полости рта. После поступления никотина в кровь происходит его распределение по органам и тканям. Больше всего он накапливается в тканях мозга, в слюне, желудочном соке, печени, легких, почках. Никотин проникает в грудное молоко через плацентарный барьер и способен накапливаться в амниотической жидкости в концентрациях, превышающих уровень концентрации никотина в сыворотке крови матери [47]. Скорость метаболизма никотина зависит от многих факторов (пол, возраст, питание, беременность), и по некоторым данным – от генетического полиморфизма цитохрома Р450 2А6 (CYP2A6), принимающего участие в метаболизме никотина. От активности цитохрома и скорости метаболизма никотина и котинина зависит поведение курящего (например, количество выкуриваемых сигарет, риск для развития зависимости и успешности прекращения курения) [26, 50]. Период полураспада никотина составляет 2 часа, а котинина около 16 часов. Уровень концентрации котинина при курении нарастает в течение дня и достигает максимума в конце курения, что обусловливает высокие концентрации котинина ночью [24]. Передозировки никотином до последнего времени были редки, особенно со смертельным исходом, за исключением случайных отравлений детей, в том числе препаратами никотинзаместительной терапии (НЗТ) или преднамеренных отравлений с целью суицида [66,55,54]. Также возможно отравление никотином рабочих, занятых на сборе листьев табака, получившее название "болезнь зеленого табака" (green tobacco sickness – GTS) [49,53]. В последние годы увеличение ассортимента, доступности никотиносодержащих лекарственных препаратов, а также электронных систем доставки никотина (электронные сигареты – е-сигареты) способствует повышению риска отравлений никотином. Обычная сигарета содержит от 9 до 30 мг никотина, при курении одной сигареты в организм попадает около 0,5-2 мг. По некоторым данным токсическая доза никотина для некурящих взрослых составляет 4-8 мг, что является смертельной дозой для детей при приеме внутрь [48]. Чаще указывается средняя летальная доза никотина для взрослых от 30 до 60 мг (от 0,5 – 1,0 мг/кг), для детей – до 10 мг. [46]. В последнее время это подвергается сомнению и приводятся сведения указывающие, что доза более 0,5 г никотина способна убить взрослого человека [61]. Симптомы передозировки никотина могут представлять собой широкий спектр расстройств, включая повышенное слюноотделение, тошноту, рвоту, потливость, головокружение, головную боль, сердцебиение; при тяжелом отравлении могут быть судороги, брадикардия с гипотонией, аритмии и нарушение дыхания. [48, 40]. Употребление табака с вредными последствиями (F17.1) Диагностические критерии, указанные в МКБ-10 для данной рубрики практически невыполнимы в силу того, что курение табака должно быть достаточно длительным, чтобы появились вредные последствия (физические или психологические), природа которых должна быть выявляемой (и описанной), то есть когда наступают клинически очевидные вредные последствия у курильщиков уже, как правило, сформирован синдром зависимости. Синдром зависимости Психические расстройства и расстройства поведения, связанные с употреблением табака, имеют код заболевания F17 по МКБ-10 [19]. В отличие от этого в оригинальной версии ICD-10 (международных клинических описаниях и диагностических рекомендациях) используется термин интоксикация никотином, никотиновая зависимость, синдром отмены никотина [59]. В диагностическое и статистическое руководство (DSM-IV) Американской психиатрической ассоциации интоксикация никотином и злоупотребление никотином не включены, а рассматривается только синдром зависимости от никотина [30]. Терминологическая неопределенность, проявляющаяся в равнозначном использовании термина табачная зависимость и никотиновая зависимость была допустима до последнего времени, но с появлением новых форм доставки никотина, основного психоактивного вещества, вызывающего привыкание и зависимость, необходимо дать более четкое определение этому термину. Несмотря на то, что другие продукты пиролиза табака обладают некоторым психоактивным действием и вносят свой вклад в патопластику синдрома отмены и обусловливают большинство серьезных соматических осложнений, связанных с курением, они не являются причиной развития собственно синдрома зависимости. Поэтому более корректным нам представляется использование названия "Психические и поведенческие расстройства, вызванные потреблением никотина" и в дальнейшим мы будем пользоваться термином никотиновая зависимость (НЗ) [11]. Критерии зависимости от никотина в МКБ-10 (ICD-10) включают в себя 3 и более симптома, наблюдающиеся на протяжении 12 месяцев:
Диагностические критерии синдрома отмены никотина: Должно быть соответствие общим критериям состояния отмены и наличие любых двух из следующих симптомов и признаков:
Представленные диагностические критерии являются достаточно сложными для применения при решении тривиальных клинических задач. Опыт показывает, что их труднее использовать, чем другие инструменты оценки НЗ, такие как тест Фагерстрема, шкала симптомов никотиновой зависимости (Nicotine Dependence Symptom Scale NDSS) и т.д., например, тест Фагерстрема имеет более широкое практическое применение, чем критерии МКБ и DSM, вероятно из-за простоты использования и возможности прогнозирования дальнейших результатов лечения [41]. Не все исследователи разделяют данную точку зрения, некоторые считают, что необходимо дальнейшие изучение для оценки надежности теста Фагерстрема, определения его чувствительности, специфичности, положительной и отрицательной прогностической ценности [41,44]. Новые диагностические критерии НЗ должны помочь в выявлении лиц, которые подвержены риску негативных последствий употребления табака, определить тех, кто нуждается в лечении, помочь определить вид вмешательства для прекращения курения и наконец, критерии зависимости должны быть полезными в области исследований. В определенной степени это отражено в новый американской классификации DSM-V. Она включает 11 критериев, которые также не лишены ряда недостатков, описанных выше, но они способны помочь более корректно оценить степень тяжести курения: время начала курения после пробуждения, тягу к курению, и тяжесть отмены никотина [41]. Синдром отмены Прекращение курения у зависимых от никотина лиц сопровождается быстрым развитием синдрома отмены, который включает в себя влечение к табаку или другим никотиносодержащим продуктам, тревогу, снижение концентрации внимания, раздражительность или беспокойство, недомогание и слабость, дисфорическое настроение, усиление кашля, афтозный стоматит, усиление аппетита, бессонницу [28]. Продолжительность синдрома отмены составляет от 7 дней до нескольких недель, иногда месяцев. Реже встречаются запоры, желудочно-кишечный дискомфорт, потливость, тремор пальцев рук, изменение артериального давления в сторону понижения и урежение частоты сердечных сокращений [7]. Выраженность этих симптомов клинически значима и приводит к рецидиву у большинства лиц, пытающихся самостоятельно отказаться от табака. Важными факторами, способствующими рецидиву курения, являются длительно существующие нарушения концентрации внимания, аффективные расстройства, психологическая связь курения с устойчивыми повторяющимися паттернами поведения, такими как, вождение автомобиля, употребление кофе, алкоголя, перерывы в работе и т.д. Медико-социальные последствия Курение табака в большинстве стран считается одной из ведущих причин предотвратимой смертности. Вред табакокурения обусловлен в первую очередь вдыханием дыма, никотин в большей степени ответственен за привыкание, за развитие зависимости от табака. В результате курения и потребления табака возникают заболевания практически всех органов и систем человека. Сложные воспалительные процессы и изменения в иммунной системе имеют решающее значение в патогенезе заболеваний, связанных с курением, таких как хроническая обструктивная болезнь легких (ХОБЛ), эмфизема легких, рак легких и атеросклероз. Чаще всего при курении развиваются болезни сердца и сосудов, дыхательной, пищеварительной, эндокринной систем, остеопороз и т.д. [15]. Сигаретный дым может быть причиной атеросклероза, тромбоза, повышения резистентности к инсулину и развития метаболического синдрома [36]. Курение табака через трубки, кальяны не снижает риск развития заболеваний, ассоциированных с табакокурением. В эксперименте на животных было показано, что вдыхание дыма кальяна 5 дней в неделю с экспозицией по 30 минут на протяжении 1 месяца приводило к значительному увеличению сопротивления дыхательных путей, воспалению, окислительному стрессу и значительному повышению карбоксигемоглобина [45]. Несмотря на попытки опровергнуть результаты исследований о негативном влиянии на здоровье курения кальяна [27], в большинстве научных публикаций доказывается связь между курением кальяна и снижением объёма форсированного выдоха за 1 секунду (ОФВ1), что свидетельствует о возможной роли курения кальяна в развитии ХОБЛ [51], подтверждаются острые и долгосрочные последствия для сердечно-сосудистой системы. При курении кальяна увеличивается частота сердечных сокращений (ЧСС) и артериальное давление (АД), может снижаться барорефлекторная чувствительность, вариабельность ритма и толерантность к физической нагрузке. К долгосрочным негативным последствиям курения кальяна относится ишемическая болезнь сердца (ИБС) [31]. Электронные сигареты (ЭС) – один из наиболее распространенных типов электронных систем доставки никотина. ЭС – это устройство для испарения жидкости, содержащей никотин, который попадает в легкие пользователю. В химической смеси кроме никотина обычно содержится пропиленгликоль и другие химикаты. Каждое устройство содержит электронную систему испарения, батареи, электронные системы управления и картриджи с жидкостью, которые испаряются. Производители сообщают, что картриджи обычно содержат от 6 до 24 мг никотина, но иногда могут содержать более 100 мг. ЕС появились в Китае в 2003 и с тех пор стали широко доступны по всему миру. Они позиционировались, как безопасный, удобный продукт для снижения вреда от курения сигарет, но химические вещества, используемые в картриджах ЭС, не были полностью изучены. Воздействие на здоровье пропиленгликоля при длительной ингаляции вызывает особое беспокойство. Потенциальные риски, которые они представляют для здоровья пользователей остаются неопределенными, так как исследования демонстрируют, что химические продукты в картриджах широко варьируют в численности и объеме [23]. Последние исследования убедительно доказывают, что вдыхаемая аэрозоль содержит очень мелкие частицы, проникающие в альвеолы и кровеносную систему, что может вызвать развитие патологических процессов. Имеются научные доказательства вредного воздействия ЭС на организм человека, не только при активном, но и при пассивном курении [1]. По мнению ряда экспертов ЭС не может считаться эффективным средством, помогающим бросить курить. В последнее время все убедительнее научные факты, что пассивное курение (ПК) является серьезной угрозой для здоровья населения. Постоянно увеличивающаяся частота заболеваний среди детей и взрослых болезнями дыхательных путей, астмой, воспалением среднего уха, синдромом внезапной детской смерти, сосудистой дисфункцией и предрасположенностью к сердечно-сосудистым заболеваниям и раку связывают с воздействием табачного дыма при ПК, который на 15% состоит из выдыхаемого дыма курильщика и на 85% из дыма тлеющей сигареты. В одном сантиметре кубическом дыма при ПК содержится несколько миллионов полужидких частиц в смеси с продуктами горения. Качественный состав основного и побочного дыма по некоторым данным совпадает, а по некоторым – вредных веществ больше в побочном дыме, химический анализ которого выявил 21 вид твердых частиц, 19 газообразных компонентов с известными канцерогенами. Наиболее изученными канцерогенными соединениями при пассивном курении являются полициклические ароматические углеводороды, нитрозамины, гетероциклические ароматические амины и другие органические соединения. Последствиями вдыхания этих соединений являются прямые (раздражающие), опосредованные (иммунологические механизмы) эффекты и мутагенез. Это доказывают результаты экспериментов по исследованию острых эффектов пассивного курения у людей. Воздействие дыма одной сигареты в течение 5 минут вызывает адгезию лейкоцитов к эндотелиальным клеткам, а в течение 20 мин активация тромбоцитов достигает уровней, аналогичным при выкуривании двух сигарет. Пассивное курение в течении 1 часа сопровождается увеличением обмена веществ и повышением секреции гормонов щитовидной железы. Два часа умеренного воздействия табачного дыма сопровождается неблагоприятными изменениями систолического артериального давления, развитием заложенности носа, раздражением и появлением ринита. Воздействие табачного дыма длительностью до 3 ч. вызывает заметные изменения в лейкоцитарной формуле, сопровождающиеся активацией иммунных клеток, а при более длительных экспозициях – окислительный стресс. Таким образом, даже кратковременное воздействие табачного дыма может вызвать значительные негативные последствия для здоровья человека [34]. Никотин является основной причиной развития зависимости у курильщиков, он взаимодействует с никотиновыми рецепторами ацетилхолина (в основном α4 β2 никотиновые рецепторы) и стимулирует дофаминергическую передачу, это в свою очередь, стимулирует систему "награды", вызывает улучшение настроения и когнитивных функций. При хронической стимуляции никотином происходит десенсибилизация ГАМК-ергических нейронов и поэтому они теряют тормозящее влияние на дофамин, что усиливает зависимость. Исследования мозга показывают, что никотин резко увеличивает активность в префронтальной коре головного мозга и зрительных систем. Никотин негативно влияет на сердце, репродуктивную систему, легкие, почки и т.д. Многие исследования продемонстрировали его канцерогенный потенциал. Никотин также вызывает повышенный окислительный стресс и апоптоз нейронов, повреждение ДНК и т.д. Подчеркивается, что никотин стимулирует вегетативную систему, увеличивается синтез гликогена из-за стимуляции α-адренорецепторов, что приводит к снижению уровня глюкозы в крови. С действием никотина связывают гастроэзофагальный рефлюкс и язвенную болезнь желудка из-за опосредованного повышения секреции кислоты в желудке и пепсиногена. Существует повышенная частота хеликобактерной инфекции у курильщиков, устойчивой к лечению. Кроме того, как известно, никотин обладает иммуносупрессивным эффектом. Поэтому даже ответ макрофагов, являющийся "первой линией обороны" против туберкулеза, становится дисфункциональным и это приводит к увеличению заболеваемости туберкулезом. Миграция фибробластов и воспалительных клеток снижается, ухудшается эпителизация, клеточная адгезия и поэтому отмечается медленное заживление ран. Поэтому к никотину, даже в качестве никотинзаместительной терапии (НЗТ), необходимо относиться серьезно и его следует использовать только под наблюдением квалифицированного персонала [42]. Воздействие никотина во время беременности связывают с неблагоприятными репродуктивными исходами, такими как, преждевременные роды и мертворождения [29]. Существует достаточно доказательств причинно-следственной связи между курением и эректильной дисфункцией [58]. Существуют, так называемые, некурительные табачные изделия. Согласно Федеральному закону Российской Федерации от 22.12.2008 № 268-ФЗ "Технический регламент на табачную продукцию" к ним относятся табачные изделия, предназначенные для сосания, жевания или нюханья и иных способов потребления, не связанных с курением – табак сосательный (снюс), табак жевательный, табак нюхательный, насвай и другие табачные изделия. В нашей стране чаще встречается насвай – вид некурительного табачного изделия, предназначенного для сосания, изготовленный из табака, извести и другого нетабачного сырья [17]. Использование бездымного (некурительного) табака присуще многим культурам по всему миру с древних времен, в том числе в Европе, Скандинавских странах, Ближнем Востоке, в Индийском континенте, США и т.д. Табачные продукты, используемые в мире, отличаются друг от друга по составу и технологии производства, но все они взаимодействуют со слизистой оболочной ротовой области. Влажный табак помещают под верхней или нижней губой, или в районе щечной десны. Сухой табак кладут в рот или вводят через нос. Постоянные пользователи жуют табак в течение нескольких часов в день [63]. Любой продукт, который содержит табак, не является безопасным для здоровья человека. Более 25 соединений в бездымном табаке могут провоцировать рак. Наиболее вредными соединениями являются табачные нитрозамины, уровень которых напрямую связан с риском развития рака. Полоний-210 – радиоактивный продукт распада радия-226 попадает в листья табака путем поглощения с поверхности почвы из удобрений. Никотин, содержащийся в жевательном табаке, также вызывает зависимость. Опасность представляют формальдегид, бензопирены, свинец. [38]. Вред бездымного (некурительного) табака связан не с раком легких и ХОБЛ, как при курении, а с поражением слизистой желудочно-кишечного тракта и ротовой области, где длительное время находится табак. Имеются исследования показывающие, что риск рака полости рта от бездымного табака является минимальным. Тем не менее, эти данные являются спорными. Это объясняется значительным различием в характеристике продуктов, вызванных разными методами обработки табачного листа и "рецептуры" изготовления [63,39]. Международное агентство по изучению рака (IARC) подтвердило, что бездымный табак является канцерогенным, показав двукратное увеличение риска рака полости рта при использовании бездымного табака в США и Канаде, пятикратное увеличение риска в Индии и других азиатских стран и увеличение риска в семь раз в Судане. В Великобритании и Европе, за исключением Швеции, использование бездымного табака встречается редко, в основном среди этнических меньшинств [37]. Диагностика Выяснение степени зависимости от никотина – одна из важных составляющих любой терапевтической стратегии. Успешность в лечении с целью прекращения курения требует лучшего понимания природы зависимости и других факторов, которые препятствуют курильщикам воздерживаться от употребления табака. Неоднозначность в отношении взаимосвязи между выраженностью никотиновой зависимости и способностью бросить курить заставляет искать инструменты, позволяющие это оценить и определить прогноз. Как мы уже указывали, в настоящий момент практически повсеместное распространение получил, так называемый, тест Фагерстрема (Fagerström Test for Nicotine Dependence – FTND) [32]. Он рекомендуется в большинстве руководств и методических пособий по лечению табачной зависимости [20]. Его простота и краткость позволяет эффективно пользоваться им широкому кругу медицинских работников для оценки степени табачной зависимости (Таблица 1). Таблица 1. Тест зависимости от никотина Фагерстрема (FTND) 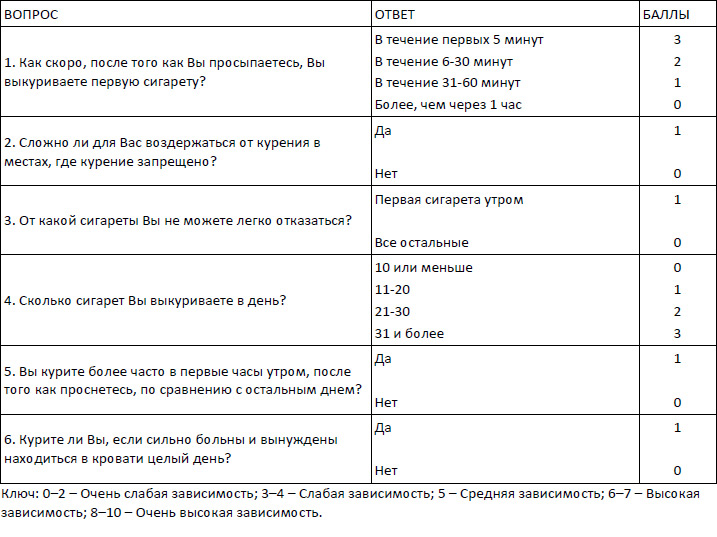 Тест Фагерстрома, как и индекс тяжести табакокурения (Heaviness of Smoking Index – HSI), являются производными от опросника толерантности Фагерстрема (Fagerström Tolerance Questionnaire FTQ). Несмотря на выявленные недостатки это теста, он помогает предсказать, насколько успешен будет отказ от курения в краткосрочной и долгосрочной перспективе. Существует мнение, что наиболее информативным является первый пункт теста – время выкуривания первой сигареты. [20]. В последнее время в связи с ростом ассортимента альтернативных табачных изделий, активной пропаганды снижения вреда от табачного дыма, проводимой во многих странах антитабачной политики, встает проблема увеличения потребления бездымного табака (smokeless tobacco – ST), для оценки тяжести которого используется модифицированный тест Фагерстрема (FTND-ST). Индекс тяжести табакокурения оперируют двумя параметрами – курению ночью, что бесспорно свидетельствует о тяжелой зависимости и количество выкуриваемых сигарет во время бодрствования. Индекс тяжести табакокурения  При диагностике тяжести зависимости необходимо учитывать наличие коморбидных наркологических заболеваний, таких как алкоголизм. В последнее время проведены сравнительные исследования, доказывающие более тяжелое течение никотиновой зависимости у больных алкоголизмом [10]. Существуют тесты, направленные на выявление уровня мотивации к отказу от курения и определению шансов успешности этого шага, несмотря на то, что ряд авторов рекомендует их использование, они не получили широкого распространения у клиницистов. Также в настоящее время используется большое количество психометрических шкал для диагностики табачной зависимости, готовности к отказу от курения и других аспектов этого заболевания, но ни одна из них не может в полной мере отразить природу табачной зависимости [9]. С другой стороны, инструмент для диагностики синдрома зависимости от табака – соответствующий раздел Международной классификаций болезней 10 пересмотра (МКБ-10) – Психические и поведенческие расстройства, вызванные потреблением табака (F. 17) представляется избыточным для специалистов общемедицинской сети, которым достаточно указать, так называемый, "курительный статус" – некурящий, бывший курильщик, случайный курильщик, курящий ежедневно, потребитель перорального табака. Для установления факта употребления табака или никотина применяются иммуно-хроматографические экспресс-тесты для определения в моче котинина – основного метаболита никотина. Определение окиси углерода в выдыхаемом воздухе (CO) – самый простой метод для мониторинга табакокурения, для этого используется газоанализатор-смокелайзер. Визуальная демонстрация степени снижения уровня угарного газа в процессе отказа от курения является хорошим стимулом для продолжения лечения, используется в качестве контроля динамики состояния, демонстрации опасности курения и эффективности здорового образа жизни. Угарный газ (CO) измеряется в ppm (частях на миллион) с помощью прилагаемой диаграммы легко преобразуются из ppm в % COHв (карбоксигемоглобина). Также используются анализаторы окиси углерода выдыхаемого воздуха с автоматическим определением карбоксигемоглобина. В норме, концентрация угарного газа в выдыхаемом воздухе у некурящего человека не должна превышать 4 ppm. Большинство курильщиков имеют более, чем 10 ppm, этот показатель коррелирует с количеством выкуриваемого табака, значимое пороговое значение для отделения курильщиков от некурящих составляет 7 ppm. [12]. Широкое используется для оценки состояния респираторной функции у курильщиков различное оборудование для исследования функции внешнего дыхания, газового состава крови и т.д. Применение этих диагностических методов и ознакомление с их результатами исследования пациентов, курящих или бросающих курить, оказывает значимое психотерапевтическое действие [28]. Для подтверждения факта курения, употребления бездымных табачных изделий или диагноза никотиновой зависимости их роль несущественна. Лечение Подходы к организации медицинской помощи лицам, употребляющим табачные изделия, в международной практике весьма сходны и основываются на рекомендациях, выработанных ВОЗ [13]. Успех ряда стран в сокращении потребления табака свидетельствует об их научной обоснованности и эффективности. Принципы лечения табачной зависимости основаны на применении кратких превентологических интервенций, когнитивно-поведенческой психотерапии (КПП), никотинзаместительной терапии (НЗТ), частичного агониста никотиновых ацетилхолиновых рецепторов (варениклин), антидепрессанта бупропиона. Стратегия помощи при табачной зависимости строится на нескольких основных принципах. Любой клиницист, имеющий непосредственное отношение к первичной медицинской помощи (врачи, медсестры, фармакологи и т.д.), которые непосредственно общаются с пациентами, должны активно выявлять курильщиков. С каждым пациентом, который курит, медицинский работник должен провести беседу о необходимости отказа от этой пагубной привычки и предложить ему лечение. Важно обеспечить курящего пациента при каждом визите хотя бы краткой беседой или информационными материалами. Используется известная модель вмешательства, получившая название "5А" – Ask /Спроси; Advise /Посоветуй; Assess/ Оцени; Assist/ Помоги; Arrange Follow-up / Организуй последующий контроль [33]. Более сжатая терапевтическая стратегия отражена в модели "АBC" (Ask about smoking status, give brief advice to quit, and offer cessation treatment (выясни курительный статус, кратко посоветуй бросить, предложи лечение, способствующее отказу от потребления табака)) [4]. Принцип краткости стратегии (беседа 3-5 минут), по мнению ряда исследователей, существенно повышает ее эффективность на уровне первичной медико-санитарной помощи, во-вторых, легче поддается стандартизации, в-третьих, по-видимому, обеспечивает сходный результат вмешательства, как и при пространных, более длительных беседах [62]. Никотинзаместительная терапия (НЗТ) Для адекватной терапии важно подобрать оптимальную дозу никотина, способ его доставки и длительность использования. Если человек выкуривает меньше 5 сигарет в сутки, то он может прекратить курение без НЗТ, если выкуривает 5-10 сигарет, то требуется в среднем 7 мг никотина, 11-17 сигарет – 14 мг никотина, 18-24 сигарет (1 пачка) – 21 мг, 2 пачки – 35 мг, более 2 пачек – 42 мг никотина в сутки. Особенности фармакодинамики различных лекарственных форм НЗТ позволяет индивидуально подобрать ту или иную схему лечения. Например, назальный спрей обеспечивает наиболее быструю доставку никотина в организм, и, следовательно, более быструю редукцию синдрома отмены, что с другой стороны повышает риск развития передозировки никотина. Он целесообразен к применению при тяжелой никотиновой зависимости [62]. Ингаляционные системы, по сути, не являются ингаляционными, а всасывание никотина происходит в полости рта, а не в альвеолах, поэтому необходимая концентрация никотина достигается более медленно, чем при курении или применении назального спрея. Вместе с тем при их применении сохраняется привычный рисунок поведения курильщика. Жевательная резинка – по фармакоэкономическим показателям наиболее доступная для большинства курящего населения форма НЗТ. Ее преимуществами является невысокий риск передозировки, возможность гибкого регулирования дозы, более быстрое, чем у трансдермальных систем, достижение необходимой концентрации никотина. Применение жевательной резинки затруднено у лиц с тяжелыми стоматологическими заболеваниями. При рекомендации больным этого вида НЗТ важно научить больного правильной технике жевания, обеспечивающей оптимальный режим поступления никотина в организм. Трансдермальные системы (пластыри) обеспечивают медленное, постоянное высвобождение никотина. В нашей стране доступны пластыри двух производителей, отличие их заключается во времени действия. В одном случае пластырь рекомендуется к применению в течение 16 часов в сутки с удалением на ночь, в другом пластырь накладывается на 24 часа. Эти различия связаны с данными о том, что большинство курильщиков не употребляют табак в ночное время и, следовательно, нет необходимости в применении НЗТ ночью. По нашему мнению, оба подхода имеют клинические основания, но при выборе того или иного продукта необходимо учитывать индивидуальные особенности и суточный ритм курения больных. Длительность НЗТ определяется индивидуально и составляет 3-6 месяцев. Комбинирование нескольких форм препаратов для НЗТ выравнивает дозу никотина и позволяет учитывать потребность конкретного больного, что способно существенно повысить эффективность терапии по сравнению проведением НЗТ на основе одного препарата. Даже сочетание нескольких форм никотинзаместительной терапии является безопасным и хорошо переносится больными. Побочные действия НЗТ редко вынуждают отменять терапию. Свидетельством высокой безопасности является решение некоторых стран, с целью повышения доступности лечения, разрешить продажу препаратов НЗТ в супермаркетах и других торговых точках [35]. Еще одним препаратом терапии первой линии является варениклин. Варениклин – частичный агонист α4β2 никотиновых ацетилхолиновых рецепторов, с двойным действием. С одной стороны, обладая более низкой внутренней силой по отношению к нАХР, по сравнению с никотином, он активирует рецептор в меньшей степени, способствуя высвобождению меньшего количества дофамина, чем при курении. С другой стороны, варениклин проявляет антагонистическое действие по отношению к никотину, так как обладает большим аффинитетом по отношению к нАХР. Таким образом, при приеме варениклина человек не испытывает привычных эффектов от курения табака и выраженных симптомов абстиненции при отказе от курения. Выброс дофамина, обусловленный действием варениклина, незначителен и поэтому не приводит к развитию зависимости от препарата [6]. Эффективность варениклина в лечении табакокурения подтверждена многочисленными исследованиями и превосходит эффективность других средств лечения зависимости от никотина, в основном за счет уменьшения вероятности рецидива курения. Варениклин предлагает вариант лечения для курильщиков, чьи потребности и возможности не рассматриваются в различных клинических руководствах, рекомендующих резко прекратить курить [43]. В Великобритании в 2008 году агентство по контролю медицинской продукции, (АКМП) опубликовало уведомление о риске развития суицидальных мыслей и поведения на фоне приема варениклина. В США в 2009 году появились предупреждения о способности варениклина (в США зарегистрирован под торговым названием Шантикс) повышать риск развития психических расстройств. В частности, FDA (Food and Drug Administration) информировало общественность о риске развития психических расстройств, которые проявлялись изменениями в поведении, ажитации, депрессивными состояниями, суицидальными попытками. Кроме того, имеется подозрение, что препарат может вызывать судороги и потерю сознания, возможно в результате внезапного нарушения сердечного ритма. Нарушения возможны и после отмены препарата. FDA до сих пор продолжает оценивать риск психоневрологических осложнений окончательные результаты ожидаются к 2017 году [64]. Эти предупреждения были основаны на спонтанных сообщениях о побочных реакциях препарата. Проведенный мета-анализ не обнаружил доказательств повышенного риска самоубийства или суицидальной активности, депрессии или смерти, связанной с приемом варениклина. В результате исследования были получены доказательства того, что варениклин скорее связан с высоким риском нарушений сна, таких как бессонница и странные сны, но эти побочные эффекты уже хорошо известны [60]. Схема приема: курильщики должны установить дату отказа от курения, желательно через неделю от начала приема варениклина. Обычная начальная доза 0,5 мг варениклина один раз в день в течение первых 3 дней, затем 0,5 мг два раза в день в течение следующих 4 дней, затем в течение недели по 0,5 мг два раза в день и с 15 дня увеличена до 1 мг два раза в день. Максимальная доза варениклина 2 мг в день. Варениклин следует принимать после еды, запивая полным стаканом воды. Рекомендованный курс лечения 12 недель. С 2010 года в Российской Федерации зарегистрирован цитизин (сейчас отпускается без рецепта), который использовался для лечения табакокурения с 60-х годов. Цитизин это растительный алкалоид, содержащийся в растениях, таких как таких как "Золотой дождь" (Cytisus Laburnum), являющееся ядовитым для человека, тем не менее, при использовании терапевтической дозы (1.5-9 мг цитизина в день) хорошо переносится при соблюдении рекомендаций, изложенных в инструкции по применению препарата. Передозировка цитизина сравнима с никотиновой интоксикацией, при которой отмечаются тошнота, рвота, расширение зрачка, тахикардия, общая слабость, клонические судороги и паралич дыхания. Привлекательность цитизина в том, что в настоящее время он относительно недорогой по сравнению с большинством других фармакологических продуктов для лечения никотиновой зависимости. Цитизин также может быть предпочтительным для тех людей, которые хотят использовать препараты на растительной основе. Фармакологическое действие цитизина похоже на действие варениклина – частичный агонист никотинового рецептора ацетилхолина. Несмотря на длительную историю использования препарата, результаты исследований эффективности цитизина не упоминаются в научной англоязычной литературе, есть только ограниченные данные клинических испытаний, проведенные до появления принципов надлежащей клинической практики (GCP). На сегодняшний день систематический обзор результатов исследований эффективности и безопасности цитизина дает основание полагать, что он имеет положительное влияние на воздержание от курения по сравнению с плацебо и достаточно безопасен [65,8]. Режим дозирования. Препарат назначают в течение 3 дней по 1 таблетки 6 раз (через 2 ч) при параллельном сокращении количества выкуриваемых сигарет. При отсутствии эффекта препарат следует отменить и через 2-3 мес. начать новый курс. При положительном результате лечение продолжают по следующей схеме: с 4 по 12 день – по 1 таблетке каждые 2.5 ч – 5 таблеток с 13 по 16 день – по 1 таблетке каждые 3 ч – 4 таблетки с 17 по 20 день – по 1 таблетке каждые 5 ч – 3 таблетки с 21 по 25 день – по 1 таблетке каждые 6-8 ч – 1-2 таблетки Курение следует прекратить не позднее 5 дня от начала лечения [7]. Бупропион также входит в первую линию терапии табачной зависимости. Более 10 лет назад бупропион был разрешен в большинстве европейских стран для лечения табакокурения. Он относится к классу психоаналептиков, селективно ингибирует обратный захват норадреналина и дофамина, а также блокирует нАХР [52]. В Российской Федерации препарат зарегистрирован, но с единственным показанием для назначения – депрессия [5]. Анксиолитики не входят в первую линию терапии зависимости от никотина, но для уменьшения раздражительности, тревоги, нарушений сна, наблюдающиеся несмотря на прием НЗТ и/или варениклина, их назначение может уменьшить вероятность возобновления курения. В настоящее время только фабомотизол – отечественный анксиолитик имеет в показаниях указание на применение для облегчения синдрома отмены при отказе от курения. Использование других анксиолитиков (транквилизаторов) будет вне зарегистрированных показаний (off label drugs). Препараты аверсивной терапии (препараты для полоскания рта, меняющие вкус дыма сигарет) в настоящее время имеют очень ограниченное использование. Необходимо отметить, что используемые до сих пор, методы лечения табакокурения без доказанной эффективности, такие как иглорефлексотерапия, гипноз, нормобарическая гипокситерапия, краниальная электростимуляция, фитотерапия, гомеопатия и пр. не рекомендуются для внедрения в практическую медицину [7,12]. Когнитивно-поведенческая психотерапия (КПП) Поведенческая терапия (в том числе краткий совет и консультирование) и фармакотерапия являются эффективными в оказании помощи людям, бросающим курить. Сочетание обоих подходов лечения рекомендуется везде, где это возможно. Индивидуальное консультирование повышает мотивацию к прекращению курения. Во время беседы врач выясняет готовность к отказу от курения, рассказывает о лечении, обсуждает с пациентом дату отказа от курения, подбирает терапию с учетом всех факторов, информирует о возможных осложнениях и трудностях, при необходимости дает рекомендации по режиму физической активности и питанию, отвечает на вопросы и назначает дату контрольного визита. Если есть возможность, предоставляет информацию о работающей телефонной линии по поддержке прекращения курения, интернет-проекте, смс-поддержке или информационные материалы [57,56]. Противорецидивное лечение Наблюдение пациента осуществляется в течение всего периода лечения, частота посещений планируется с учетом курительного статуса, сопутствующих заболеваний, выраженности мотивации на отказ от курения и других факторов. Одним из важных контрольных посещений является первое после прекращения курения (2-3 сутки), для коррекции терапии, предотвращения рецидива курения и мотивирование на дальнейшее воздержание от курения. Рецидив определяется как курение ≥ 7 сигарет в течение недели, при курении меньшего количества табака определяется, как срыв. При возникновении срыва необходимо: увеличить частоту и длительность сеансов КПТ и/или использовать более длительный срок (более 14 недель) комбинированную НЗТ и/или продлить применение варениклина с 12 до 24 недель для предотвращения рецидива и возвращения состояния ремиссии [12]. Важно обращать внимание на сопутствующую соматическую патологию, особенно на обострение хронического бронхита, клиника которого появляется примерно через неделю отказа от курения. Усиление кашля и затруднения отхождения мокроты могут послужить провоцирующим фактором для возобновления курения, поэтому о возможном появлении респираторных симптомов необходимо предупредить пациента и при необходимости направить на клиническое обследование и оценку функции внешнего дыхания с целью выявления гиперреактивности бронхов или бронхиальной обструкции. При обнаружении признаков хронического бронхита целесообразно назначение муколитиков (ацетилцистеина) и бронхорасширяющих препаратов: бета2-адреномиметика пролонгированного действия (формотерола фумарат) и/или М-холиноблокатора пролонгированного действия (тиотропия бромид). Лечение респиратоных симптомов улучшает самочувствие пациента и повышает эффективность лечения табакокурения [14]. Список литературы 1. Антонов Н.С., Сахарова Г.М., Донитова В.В., Котов А.А., Бережнова И.А., Латиф Э. Электронные сигареты: оценка безопасности и рисков для здоровья// Пульмонология. – 2014. – № 3.- С.122-127. 2. ВЦИОМ. Пресс-выпуск № 3116. Режим доступа: http://wciom.ru/index.php?id=236&uid=115711 3. Доклад ВОЗ о глобальной табачной эпидемии, 2009 год. Создание среды, свободной от табачного дыма // Режим доступа: http://whqlibdoc.who.int/publications/2010/9789244563915_rus.pdf 4. Доклад о табачной зависимости и прекращении употребления табака (в связи со статьей 14 Конвенции (решение FCTC/COP 2 (14)) //ВОЗ. – 2008. – 22с. 5. Инструкция по применению лекарственного препарата для медицинского применения Веллбутрин // Государственный реестр лекарственных средств. – Режим доступа: http://grls.rosminzdrav.ru/InstrImgMZ.aspx?regNr=ЛСР-008003/10&page=2 6. Кукес В.Г., Маринин В.Ф., Гаврисюк Е.В. Варениклин – препарат нового поколения для лечения табачной зависимости //Клиническая фармакология и терапия – 2009. – Т 18. – №3. – С.1-5. 7. Левшин В.Ф. Табакизм: патогенез, диагностика и лечение. – М.: ИМА-ПРЕСС, – 2012, – 128с. 8. Левшин В.Ф., Слепченко Н.И., Радкевич Н.В. Рандомизированное контролируемое исследование эффективности препарата Табекс® (цитизин) при лечении табачной зависимости. / Вопросы наркологии. – 2009. – №5. – С. 13-22. 9. Махов М.А. Табачная зависимость – инструменты измерения // Наркология – 2015. – №3. – С.46 – 57. 10. Махов М.А., Надеждин А.В. Клинические особенности табачной зависимости у больных алкоголизмом // Наркология. – 2016. – №1. – С. 39 – 50. 11. Надеждин А.В., Тетенова Е.Ю., Зекрина Н.А., Колгашкин А.Ю. Лечение и диагностика никотиновой зависимости// Наркология. – 2011. – Т. 10. – № 10 (118). – С. 84-94. 12. Прекращение потребления табака и лечение табачной зависимости. Научно обоснованные рекомендации под редакцией профессора А.К. Демина. Москва, Российская Федерация – Вашингтон, округ Колумбия, США, Издательство: РАПСИГО. – 2013.- 244 с. 13. Рамочная конвенция ВОЗ по борьбе против табака. – 2003. – 42с. – Режим доступа: http://www.who.int/fctc/whofctc_cover_russian.pdf 14. Сахарова Г.М., Антонов Н.С. Оказание помощи по отказу от табака в терапевтической практике //Учебное пособие. – 2010.- "УП Принт" Россия, Москва – 64с. 15. Сахарова Г.М., Антонов Н.С. Вредное воздействие табакокурения на здоровье и подходы к лечению табачной зависимости//"Справочник поликлинического врача", – 2008. – № 14–15, – C. 16-20 16. Федеральный закон от 23 февраля 2013 г. N 15-ФЗ "Об охране здоровья граждан от воздействия окружающего табачного дыма и последствий потребления табака". // режим доступа: https://rg.ru/2013/02/26/zakon-dok.html 17. Федеральный закон Российской Федерации от 22.12.2008 № 268-ФЗ "Технический регламент на табачную продукцию" // "Российская газета" – Федеральный выпуск №4822. – режим доступа: http://www.rg.ru/2008/12/26/tabak-dok.html 18. Фонд Общественное мнение (24-25.10.15). О курении и дыхании. Режим доступа: http://fom.ru/Zdorove-i-sport/12483 19. Чуркин А.А., Мартюшов А.Н. Краткое руководство по использованию МКБ-10 в психиатрии и наркологии. М.: Издательство "Триада –Х" – 1999. – С.28-36. 20. Чучалин А.Г., Сахарова Г.М., Антонов Н.С., Зайцева О.Ю., Новиков К.Ю. Комплексное лечение табачной зависимости и профилактика хронической обструктивной болезни легких, вызванной курением табака. Методические рекомендации Министерства здравоохранения и социального развития. – 2003. – № 2002/154. – 48 с. 21. Baker T.B., Breslau N., Covey L., Shiffman S. DSM Criteria for Tobacco Use Disorder and Tobacco Withdrawal: A Critique and Proposed Revisions for DSM-5.//Addiction. – 2013. – V.107.- №2. Р. 263–275. doi: 10.1111/j.1360-0443.2011.03657.x 22. Baker Т.B., Piper M.E., McCarthy D.E., Bolt D.M., et al. Time to first cigarette in the morning as an index of ability to quit smoking: Implications for nicotine dependence// Nicotine Tob. Res. – 2007. – V.9. – №4. – P.555–570. doi: 10.1080/14622200701673480 23. Bam T. S., Bellew W., Berezhnova I., Jackson-Morris A., Jones A., Latif E., Molinari M. A., Quan G., Singh R. J., Wisotzky M. Position statement on electronic cigarettes or electronic nicotine delivery systems// International Union Against Tuberculosis and Lung Disease. – 2014. – V.18. – № 1. – P.5–7. http://dx.doi.org/10.5588/ijtld.13.0815 24. Benowitz N.L. Cotinine as a Biomarker of Environmental Tobacco Smoke Exposure // Epidemiol. Rev. – 1996. – Vol. 18, – №.2. – P.188-204. 25. Benowitz N.L., Hukkanen J., Jacob P., Nicotine Chemistry, Metabolism, Kinetics and Biomarkers// Handbook of Experimental Pharmacology. – 2009. – Vol.192. – P. 29 – 60. 26. Bloom J., Hinrichs A.L., Wang J.C., von Weymarn L.B., Kharasch E.D., Bierut L.J., Goate A., Murphy S.E. The contribution of common CYP2A6 alleles to variation in nicotine metabolism among European-Americans.//Pharmacogenet Genomics. – 2011.- V.21, №7.- P.403-416. doi: 10.1097/FPC.0b013e328346e8c0. 27. Chaouachi K. Use & Misuse of Water-filtered Tobacco Smoking Pipes in the World. Consequences for Public Health, Research & Research Ethics//Open Med Chem. J. – 2015. – № 9. – Р. 1–12. doi: 10.2174/1874104501509010001 28. Clinical guidelines and procedures for the management of nicotine dependent inpatients //Department of Health, Western Australia. – 2011. P. 2. 29. Clinical guidelines and procedures for the management of nicotine dependent inpatients //Department of Health, Western Australia. – 2011. P. 9. 30. Diagnostic and statistical manual of mental disorders: DSM-IV. – 4th ed. /American Psychiatric Association – Washington, -1994. – P. 242-247. 31. El-Zaatari Z.M. Chami H.A., Zaatari G.S. Health effects associated with waterpipe smoking//Tob. Control. – 2015. – V. 24. -№ 1. P.31–43. doi: 10.1136/tobaccocontrol-2014-051908 32. Fagerstrom K.O., Schneider N. Measuring nicotine dependence: a review of the Fagerstrom Tolerance Questionnaire. J. Behav. Med. – 1989. – №12. – Р. 159–182 33. Fiore M.C., Bailey W.C., Cohen S.J., et al. Treating Tobacco Use and Dependence/ Clinical Practice Guideline. – Rockville, Md: US Department of Health and Human Services. Public Health Service. – 2000. 34. Flouris A.D., Vardavas C.I., Metsios G.S., Tsatsakis A.M., Koutedakis Y. Biological evidence for the acute health effects of secondhand smoke exposure//American Journal of Physiology – Lung Cellular and Molecular Physiology Published. – 2010. – Vol. 298. – №1. – С.3-12. doi: 10.1152/ajplung.00215.2009 35. Framework for the treatment of nicotine addiction. Perth: Health Networks Branch, Department of Health, Western Australia. – 2010. 36. Global Heart 2012 / World Heart Federation (Geneva). Published by Elsevier Ltd. All rights reserved. – 2012, – Vol.7. – №.2. doi:10. 1016/j.gheart.2012.05.003 37. Hashemipour M.A., Gholampour F., Fatah F., Bazregari S. Snus (nass) and oral cancer: A case series report// Dent Res J (Isfahan). – 2013. – V.10. – №1. – Р.116–121. doi: 10.4103/1735-3327.111813 38. International Agency for Research on Cancer. Vol. 89. Lyon, France: World Health Organization International Agency for Research on Cancer; IARC Monographs on the Evaluation of Carcinogenic Risks to Humans; 2007. Smokeless Tobacco and Some Tobacco-Specific N-Nitrosamines. 39. Lee Р. Summary of the epidemiological evidence relating snus to health//Regul. Toxicol. Pharmacol. – 2011. – №59. – Р. 197–214 40. Mayer B. How much nicotine kills a human? Tracing back the generally accepted lethal dose to dubious self-experiments in the nineteenth century//Arch. Toxicol. – 2014. –V. 88, – №1. – Р. 5–7. 41. Meneses-Gaya I.C., Zuardi A.W., Loureiro S.R., Crippa J.A. Psychometric properties of the Fagerström Test for Nicotine Dependence.//J Bras Pneumol. 2009. – 35(1):73-82. 42. Mishra A., Chaturvedi P., Datta S., Sinukumar S., Joshi P., Garg A. Harmful effects of nicotine//Indian J. Med Paediatr. Oncol. – 2015. – V.36. – №1. – Р.24–31. doi: 10.4103/0971-5851.151771 43. Munarini Е., Marabelli C., Pozzi P., Boffi R. Extended varenicline treatment in a severe cardiopathic cigarette smoker: a case report//J. Med. Case Rep. 2015. – V. 9:29. doi: 10.1186/1752-1947-9-29 44. Mushtaq N., Beebe L.A. A review of the validity and reliability of smokeless tobacco dependence measures.// Addict. Behav. -2012. – V.37. – №4. – Р.361-366. doi: 10.1016/j.addbeh.2011.12.003. 45. Nemmar A., Raza H., Yuvaraju P., Beegam S., John A., Yasin J. , Rasheed S. et al. Nose-only water-pipe smoking effects on airway resistance, inflammation, and oxidative stress in mice// Journal of Applied Physiology. – 2013, -Vol. 115. – №9..- Р.1316-1323 doi: 10.1152/japplphysiol.00194.2013 46. Nicotine//IPCS INCHEM. Режим доступа: http://www.inchem.org/documents/pims/chemical/nicotine.htm#PartTitle:1. NAME 47. NIDA Tobacco Addiction. – 2009. – 12c. – Mode of access: http://smoking.drugabuse.gov 48. Novotny T.E., Hardin S.N., Hovda L.R., Novotny D.J., McLean M.K., Khan S. Tobacco and cigarette butt consumption in humans and animals//Tob. Control. – 2011. – V. 20. – №1. – P.17–20. doi: 10.1136/tc.2011.043489 49. Oliveira P.P, Sihler C.B., Moura L., et al. First reported outbreak of green tobacco sickness in Brazil// Cad. Saude Publica. – 2010. – №12. – P. 2263 – 2269, 50. Piliguian M., Zhu A.Z., Zhou Q., Benowitz N.L., Ahluwalia J.S., Sanderson Cox L., Tyndale R.F. Novel CYP2A6 variants identified in African Americans are associated with slow nicotine metabolism in vitro and in vivo.//Pharmacogenet. Genomics. – 2014. V.24,- №2. – P.118-28. doi: 10.1097/FPC.0000000000000026. 51. Raad D., Gaddam S., Schunemann H.J., Irani J., Abou Jaoude P., Honeine R., Akl E.A. Effects of water-pipe smoking on lung function: a systematic review and meta-analysis.//Chest.- 2011. – V. 139. – №4. – P. 764-74. doi: 10.1378/chest.10-0991. 52. Raupach T., Schayck C.P. Pharmacotherapy for Smoking Cessation//CNS Drugs. – 2011. – Vol. 25. – №5. – P. 371 – 382. 53. Satora L., Goszcz H., Gomółka E., Biedroń W. Green tobacco sickness in Poland.//Pol. Arch. Med. Wewn. – 2009. – V.119, – № 3. – Р.184-6. Режим доступа: http://pamw.pl/sites/default/files/satora_en.pdf 54. Saxena K., Scheman A.Suicide plan by nicotine poisoning: a review of nicotine toxicity.//Vet Hum Toxicol. – 1985. – V.27.-№6. – Р.495-7. Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/4082460 55. Smolinske S.C., Spoerke D.G., Spiller S.K., Wruk K.M., Kulig K., Rumack B.H.Cigarette and nicotine chewing gum toxicity in children.//Hum Toxicol. – 1988. – V.7, – №1.- P.27-31. 56. Stead L.F., Hartmann-Boyce J., Perera R., Lancaster T. Telephone counselling for smoking cessation.//Cochrane Database Syst. Rev. – 2013. – 12;8:CD002850. doi: 10.1002/14651858.CD002850.pub3. 57. Stead L.F., Lancaster T. Combined pharmacotherapy and behavioural interventions for smoking cessation.//Cochrane Database Syst Rev. – 2012. – Oct 17;10:CD008286. doi: 10.1002/14651858.CD008286.pub2. 58. The Health Consequences of Smoking – 50 Years of Progress: A Report of the Surgeon General. Atlanta, GA: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Center for Chronic Disease Prevention and Health Promotion, Office on Smoking and Health, 2014. – P.8-10. 59. The ICD-10 Classification of Mental and Behavioural Disorders. Режим доступа: http://www.who.int/classifications/icd/en/GRNBOOK.pdf?ua=1 60. Thomas K.H., Martin R.M., Knipe D.W., Higgins J.P., Gunnell D. Risk of neuropsychiatric adverse events associated with varenicline: systematic review and meta-analysis//BMJ. – 2015. – V. 12. – № 350:h1109. doi: 10.1136/bmj.h1109. 61. Tonstad S., Gustavsson G., Kruse E., Walmsley J.M., Westin A. Symptoms of nicotine toxicity in subjects achieving high cotinine levels during nicotine replacement therapy.// Nicotine Tob. Res. – 2014. – V.16, – №9. – Р.1266-71. doi: 10.1093/ntr/ntu076. Epub 2014 May 22. 62. Treating Tobacco Use and Dependence: 2008 Update U.S. Department of Health and Human Services Public Health Service May 2008. – Mode of access: http://www.surgeongeneral.gov/tobacco/treating_tobacco_use08.pdf 63. Underner M., Perriot J., Peiffer G. Smokeless tobacco// Presse Med. – 2012. – №41(1).– Р. 3-9. doi: 10.1016/j.lpm.2011.06.005. 64. Varenicline (marketed as Chantix) Information//U.S. Food and Drug Administration. режим доступа: http://www.fda.gov/Drugs/DrugSafety/ PostmarketDrugSafetyInformationforPatientsandProviders/ucm106540.htm 65. Walker N., Howe C., Bullen C., McRobbie H., Glover M., et al Study protocol for a non-inferiority trial of cytisine versus nicotine replacement therapy in people motivated to stop smoking//BMC Public Health. – 2011. – № 11: 880. doi: 10.1186/1471-2458-11-880 66. Woolf A., Burkhart K., Caraccio T., Litovitz T. Childhood poisoning involving transdermal nicotine patches.//Pediatrics. – 1997. – V.99, – №5.: E4. Режим доступа: http://www.ncbi.nlm.nih.gov/pubmed/9113961
Abstract The paper presents the diagnostic criteria of ICD-10 for major morbid conditions associated with the use of nicotine. Authors consider health and social consequences of tobacco use by means of pipes and hookahs, harm associated with passive smoking, use of electronic cigarettes and smokeless forms of tobacco. Principal tools for the diagnosis of the degree of dependence syndrome and readiness to quit, as well as modern treatment methods are presented. Key words Tobacco dependence, tobacco use, nicotine dependence, electronic cigarettes, passive smoking, nicotine replacement therapy, Fagerstrom test References 1. Antonov N.S., Saharova G.M., Donitova V.V., Kotov A.A., Berezhnova I.A., Latif E, "Electronic cigarettes: evaluation of safety and health risks." Pulmonologiya 3 (2014): 122-27. 2. VCIOM, Press release № 3116. Accessed at: http://wciom.ru/index.php?id=236&uid=115711 3. WHO report on global tobacco epidemic, 2009: implementing smoke-free environments. Accessed at: http://whqlibdoc.who.int/publications/2010/9789244563915_rus.pdf 4. Report on tobacco dependence and cessation (in accordance with Article 14 of Convention (FCTC/COP 2 (14)). WHO, 2008. Print. 5. Instructions for use of Wellbutrin. State Register of Medicinal Products. Accessed at: http://grls.rosminzdrav.ru/InstrImgMZ.aspx?regNr=ЛСР-008003/10&page=2 6. Kukes V.G., Marinin V.F., Gavrisyuk E.V, "Varenicline – the new generation drug for the treatment of tobacco dependence." Klinicheskaya farmakologiya i terapiya 3 (2009): 1-5. 7. Levshin V.F, Tobacco dependence: pathogenesis, diagnosis and treatment. Moscow: IMA-PRESS, 2012. Print. 8. Levshin V.F., Slepchenko N.I., Radkevich N.V, "A randomized controlled efficacy study of Tabeks® (cytisine) for the treatment of tobacco dependence." Voprosy narkologii 5 (2009): 13-22. 9. Mahov M.A, "Measuring tools for tobacco dependence." Narkologiya 3 (2015): 46-57. 10. Mahov M.A., Nadezhdin A.V, "Clinical features of tobacco dependence in patients with alcohol addiction." Narkologiya 1 (2016): 39-50. 11. Nadezhdin A.V., Tetenova E.Yu., Zekrina N.A., Kolgashkin A.Yu, "Treatment and diagnosis of nicotine dependence." Narkologiya 10 (2011): 84-94. 12. Smoking cessation and treatment of tobacco dependence. Evidence-based recommendations edited by Professor A.K. Demin. Moscow – Washington DC. Moscow: RAPSIGO, 2013. Print. 13. WHO Framework Convention on Tobacco Control. Accessed at: http://www.who.int/fctc/whofctc_cover_russian.pdf 14. Saharova G.M., Antonov N.S, Facilitating smoking cessation in therapeutic practice. Textbook. Moscow: UP Print, 2010. Print. 15. Saharova G.M., Antonov N.S, "The harmful effects of smoking on health and the approaches to the treatment of tobacco dependence." Spravochnik poliklinicheskogo vracha 14-15 (2008): 16-20. 16. Federal Law of 23 February 2013 N 15-FZ "On the Protection of the health of citizens from exposure to tobacco smoke and the consequences of tobacco use." Accessed at: https://rg.ru/2013/02/26/zakon-dok.html 17. Federal Law of the Russian Federation of 22.12.2008 number 268-FZ "Technical Regulations on Tobacco Products." Accessed at: http://www.rg.ru/2008/12/26/tabak-dok.html 18. "Public Opinion" Foundation (24-25.10.2015). On smoking and breath. Accessed at: http://fom.ru/Zdorove-i-sport/12483 19. Churkin A.A., Martyushov A.N, Quick guide to using the ICD-10 in mental health and addiction. Moscow: Triada-X, 1999. Print. 20. Chuchalin A.G., Saharova G.M., Antonov N.S., Zajceva O.Yu., Novikov K.Yu, Comprehensive treatment of tobacco dependence and prevention of chronic obstructive pulmonary disease caused by tobacco smoking. Methodical guidelines of the Ministry of Health and Social Development. Moscow, 2002. Print. 21. Baker T.B., Breslau N., Covey L., Shiffman S. "DSM Criteria for Tobacco Use Disorder and Tobacco Withdrawal: A Critique and Proposed Revisions for DSM-5." Addiction 2 (2013): 263-75. doi: 10.1111/j.1360-0443.2011.03657.x. 22. Baker Т.B., Piper M.E., McCarthy D.E., Bolt D.M., et al. "Time to first cigarette in the morning as an index of ability to quit smoking: Implications for nicotine dependence." Nicotine Tob. Res. 4 (2007): 555-70. doi: 10.1080/14622200701673480. 23. Bam T. S., Bellew W., Berezhnova I., Jackson-Morris A., Jones A., Latif E., Molinari M. A., Quan G., Singh R. J., Wisotzky M. "Position statement on electronic cigarettes or electronic nicotine delivery systems." International Union Against Tuberculosis and Lung Disease 1 (2014): 5-7. 24. Benowitz N.L. "Cotinine as a Biomarker of Environmental Tobacco Smoke Exposure." Epidemiol. Rev. 2 (1996): 188-204. 25. Benowitz N.L., Hukkanen J., Jacob P., "Nicotine Chemistry, Metabolism, Kinetics and Biomarkers." Handbook of Experimental Pharmacology Vol.192 (2009): 29-60. 26. Bloom J., Hinrichs A.L., Wang J.C., von Weymarn L.B., Kharasch E.D., Bierut L.J., Goate A., Murphy S.E. "The contribution of common CYP2A6 alleles to variation in nicotine metabolism among European-Americans." Pharmacogenet Genomics. 7 (2011): 403-16. doi: 10.1097/FPC.0b013e328346e8c0. 27. Chaouachi K. "Use & Misuse of Water-filtered Tobacco Smoking Pipes in the World. Consequences for Public Health, Research & Research Ethics." Open Med Chem. J. 9 (2015): 1-12. doi: 10.2174/1874104501509010001/. 28. Clinical guidelines and procedures for the management of nicotine dependent inpatients. Department of Health, Western Australia. 2011. P. 2. Print. 29. Clinical guidelines and procedures for the management of nicotine dependent inpatients. Department of Health, Western Australia. 2011. P. 9. Print. 30. Diagnostic and statistical manual of mental disorders: DSM-IV. – 4th ed. American Psychiatric Association – Washington, – 1994. Print. 31. El-Zaatari Z.M. Chami H.A., Zaatari G.S. "Health effects associated with waterpipe smoking." Tob. Control. 1 (2015): 31-43. doi: 10.1136/tobaccocontrol-2014-051908. 32. Fagerstrom K.O., Schneider N. "Measuring nicotine dependence: a review of the Fagerstrom Tolerance Questionnaire." J. Behav. Med. 12 (1989): 159-182. 33. Fiore M.C., Bailey W.C., Cohen S.J., et al. Treating Tobacco Use and Dependence. Clinical Practice Guideline. – Rockville, Md: US Department of Health and Human Services. Public Health Service. – 2000. Print. 34. Flouris A.D., Vardavas C.I., Metsios G.S., Tsatsakis A.M., Koutedakis Y. "Biological evidence for the acute health effects of secondhand smoke exposure." American Journal of Physiology – Lung Cellular and Molecular Physiology 1 (2010): 3-12. doi: 10.1152/ajplung.00215.2009/. 35. Framework for the treatment of nicotine addiction. Perth: Health Networks Branch, Department of Health, Western Australia. – 2010. Print. 36. Global Heart 2012 / World Heart Federation (Geneva). 2 (2012). doi:10. 1016/j.gheart.2012.05.003. 37. Hashemipour M.A., Gholampour F., Fatah F., Bazregari S. "Snus (nass) and oral cancer: A case series report." Dent Res J (Isfahan) 1 (2013): 116-21. doi: 10.4103/1735-3327.111813 38. International Agency for Research on Cancer. Vol. 89. Lyon, France: World Health Organization International Agency for Research on Cancer; IARC Monographs on the Evaluation of Carcinogenic Risks to Humans; 2007. Smokeless Tobacco and Some Tobacco-Specific N-Nitrosamines. 39. Lee Р. "Summary of the epidemiological evidence relating snus to health." Regul. Toxicol. Pharmacol. 59 (2011): 197-214. 40. Mayer B. "How much nicotine kills a human? Tracing back the generally accepted lethal dose to dubious self-experiments in the nineteenth century." Arch. Toxicol. 1 (2014): 5-7. 41. Meneses-Gaya I.C., Zuardi A.W., Loureiro S.R., Crippa J.A. "Psychometric properties of the Fagerström Test for Nicotine Dependence." J Bras Pneumol. 1 (2009): 73-82. 42. Mishra A., Chaturvedi P., Datta S., Sinukumar S., Joshi P., Garg A. "Harmful effects of nicotine." Indian J. Med Paediatr. Oncol. 1 (2015): 24-31. doi: 10.4103/0971-5851.151771. 43. Munarini Е., Marabelli C., Pozzi P., Boffi R. "Extended varenicline treatment in a severe cardiopathic cigarette smoker: a case report." J. Med. Case Rep. V. 9:29 (2015). doi: 10.1186/1752-1947-9-29 44. Mushtaq N., Beebe L.A. "A review of the validity and reliability of smokeless tobacco dependence measures." Addict. Behav. 4 (2012): 361-6. doi: 10.1016/j.addbeh.2011.12.003. 45. Nemmar A., Raza H., Yuvaraju P., Beegam S., John A., Yasin J., Rasheed S. et al. "Nose-only water-pipe smoking effects on airway resistance, inflammation, and oxidative stress in mice." Journal of Applied Physiology 9 (2013): 1316-23 doi: 10.1152/japplphysiol.00194.2013. 46. Nicotine. IPCS INCHEM. Accessed at: http://www.inchem.org/documents/pims/chemical/nicotine.htm#PartTitle:1. NAME 47. NIDA Tobacco Addiction. – 2009. Accessed at: http://smoking.drugabuse.gov 48. Novotny T.E., Hardin S.N., Hovda L.R., Novotny D.J., McLean M.K., Khan S. "Tobacco and cigarette butt consumption in humans and animals." Tob. Control. 1 (2011): 17-20. doi: 10.1136/tc.2011.043489. 49. Oliveira P.P, Sihler C.B., Moura L., et al. "First reported outbreak of green tobacco sickness in Brazil." Cad. Saude Publica. 12 (2010): 2263-69. 50. Piliguian M., Zhu A.Z., Zhou Q., Benowitz N.L., Ahluwalia J.S., Sanderson Cox L., Tyndale R.F. "Novel CYP2A6 variants identified in African Americans are associated with slow nicotine metabolism in vitro and in vivo." Pharmacogenet. Genomics. 2 (2014): 118-28. doi: 10.1097/FPC.0000000000000026. 51. Raad D., Gaddam S., Schunemann H.J., Irani J., Abou Jaoude P., Honeine R., Akl E.A. "Effects of water-pipe smoking on lung function: a systematic review and meta-analysis." Chest. 4 (2011): 764-74. doi: 10.1378/chest.10-0991. 52. Raupach T., Schayck C.P. "Pharmacotherapy for Smoking Cessation." CNS Drugs 5 (2011): 371-82. 53. Satora L., Goszcz H., Gomółka E., Biedroń W. "Green tobacco sickness in Poland." Pol. Arch. Med. Wewn. 3 (2009): 184-6. 54. Saxena K., Scheman A. "Suicide plan by nicotine poisoning: a review of nicotine toxicity." Vet Hum Toxicol. 6 (1985): 495-7. 55. Smolinske S.C., Spoerke D.G., Spiller S.K., Wruk K.M., Kulig K., Rumack B.H. "Cigarette and nicotine chewing gum toxicity in children." Hum Toxicol. 1 (1988): 27-31. 56. Stead L.F., Hartmann-Boyce J., Perera R., Lancaster T. "Telephone counselling for smoking cessation." Cochrane Database Syst. Rev. – 2013. – 12;8:CD002850. doi: 10.1002/14651858.CD002850.pub3. 57. Stead L.F., Lancaster T. "Combined pharmacotherapy and behavioural interventions for smoking cessation." Cochrane Database Syst Rev. – 2012. – Oct 17;10:CD008286. doi: 10.1002/14651858.CD008286.pub2. 58. The Health Consequences of Smoking – 50 Years of Progress: A Report of the Surgeon General. Atlanta, GA: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Center for Chronic Disease Prevention and Health Promotion, Office on Smoking and Health, 2014. – P.8-10. Print. 59. The ICD-10 Classification of Mental and Behavioural Disorders. Accessed at: http://www.who.int/classifications/icd/en/GRNBOOK.pdf?ua=1 60. Thomas K.H., Martin R.M., Knipe D.W., Higgins J.P., Gunnell D. "Risk of neuropsychiatric adverse events associated with varenicline: systematic review and meta-analysis." BMJ 2015. V. 12. № 350:h1109. doi: 10.1136/bmj.h1109. 61. Tonstad S., Gustavsson G., Kruse E., Walmsley J.M., Westin A. "Symptoms of nicotine toxicity in subjects achieving high cotinine levels during nicotine replacement therapy." Nicotine Tob. Res. 9 (2014): 1266-71. doi: 10.1093/ntr/ntu076. Epub 2014 May 22. 62. Treating Tobacco Use and Dependence: 2008 Update U.S. Department of Health and Human Services Public Health Service May 2008. Accessed at: http://www.surgeongeneral.gov/tobacco/treating_tobacco_use08.pdf 63. Underner M., Perriot J., Peiffer G. "Smokeless tobacco." Presse Med. 1 (2012): 3-9. doi: 10.1016/j.lpm.2011.06.005. 64. Varenicline (marketed as Chantix) Information//U.S. Food and Drug Administration. Accessed at: http://www.fda.gov/Drugs/DrugSafety/ PostmarketDrugSafetyInformationforPatientsandProviders/ucm106540.htm 65. Walker N., Howe C., Bullen C., McRobbie H., Glover M., et al "Study protocol for a non-inferiority trial of cytisine versus nicotine replacement therapy in people motivated to stop smoking." BMC Public Health 11 (2011): 880. doi: 10.1186/1471-2458-11-880 66. Woolf A., Burkhart K., Caraccio T., Litovitz T. "Childhood poisoning involving transdermal nicotine patches." Pediatrics 5 (1997): E4. |
[ См. также ] Рубрики |
||||
|
|
|
Журнал «Медицина» © ООО "Инновационные социальные проекты"
|