| О журнале | Редколлегия | Редсовет | Архив номеров | Поиск | Авторам | Рецензентам | English |
Использование препарата Креон® Микро в терапии экзокринной недостаточности поджелудочной железы у детей с муковисцидозом. Анализ влияния на бюджет.
Дата публикации 15 апреля 2017 года. Аннотация В работе рассматривается проблема выбора наиболее адекватных препаратов для заместительной терапии эндокринной недостаточности поджелудочной железы. Оцениваются возможные последствия для бюджета Российской Федерации от включения в списки ЖНВЛП нового препарата для заместительной терапии – Креон® Микро. Делается вывод о том, что широкое применение данного препарата позволит достичь значительной экономии бюджета при сохранении эффективности лечения. Ключевые слова муковисцидоз, ферментная терапия, Креон® Микро, панкреатические ферменты, кишечнорастворимые капсулы Муковисцидоз (кистозный фиброз) – это наследственное заболевание, вызванное наличием аутосомно-рецессивной мутации и поражающее железы внешней секреции, что приводит к развитию патологии органов дыхания и желудочно-кишечного тракта. В Российской Федерации частота рождения детей с муковисцидозом составляет примерно 1 на 10000. Расходы на терапию муковисцидоза достаточно велики. Согласно австралийским данным [1], среднегодовые расходы на терапию пациента с муковисцидозом составляют 15571 доллар США, а расходы в течение всей жизни составляют 306332 доллара США с учетом 3,5% дисконтирования. Расходы на лечение в Чешской Республике составляют 14486 евро на человека [2], в Германии – 41468 евро на человека [3], а по данным итальянских авторов сумма варьировала от 4164 евро на человека в год до более чем 30 тысяч евро в год [4]. Патология поджелудочной железы характерна для муковисцидоза и приводит к развитию экзокринной недостаточности с неспособностью больными переваривать и усваивать жиры. В результате отсутствия заместительной ферментной терапии нутритивный статус пациентов с муковисцидозом ухудшается, наблюдается задержка развития и усугубляется другая патология. Дело в том, что между нутритивным статусом пациента и тяжестью заболевания существует тесная связь – подростки с муковисцидозом и плохим нутритивным статусом демонстрировали падение объема форсированного выдоха (ОФВ1) примерно на 20%, тогда как при хорошем статусе он оставался стабильным [5]. Проспективное наблюдение показало, что лица, у которых наблюдалось снижение относительной массы тела (по сравнению с возрастными нормами) более, чем на 5% одновременно демонстрировали падение ОФВ1 на 16,5% [5]. Это важное наблюдение, не только с клинической, но и с экономической точки зрения, поскольку было показано, что увеличение ОФВ1 на 1% приводило к снижению расходов на 0,9% в отношении медицинских продуктов, 1,7% для суммарных расходов, 2,8% расходов на различные процедуры и на 7% расходов на госпитализацию [2]. Вместе с тем, расходы на ферментную терапию у взрослых пациентов с муковисцидозом по своим размерам уступают только расходам на дорназу альфа [1], обгоняя по стоимости расходы на антибактериальную терапию. По этой причине выбор наиболее адекватных препаратов для заместительной терапии экзокринной недостаточности поджелудочной железы является важным вопросом. Целью данного исследования было оценить возможные последствия для бюджета Российской Федерации от включения в списки ЖНВЛП нового препарата для заместительной терапии – Креон® Микро. Новая лекарственная форма данного препарата специально разработана для заместительной терапии у детей и, в первую очередь, у детей с муковисцидозом [6]. Препарат представляет собой кишечнорастворимые гранулы, содержащие в 100 мг препарата (объем прилагаемой мерной ложечки) 60,12 мг свиного панкреатина 5000 ед. липазы, 3600 ед. амилазы и 200 ед. протеазы, во флаконе, содержащем 20 г препарата Данная лекарственная форма позволяет более точно подобрать индивидуальную дозу с более низкой активностью липазы, что необходимо для адекватного лечения детей. Гранулы можно добавлять к небольшому количеству мягкой пищи, не требующей пережевывания и имеющей кислый вкус, или принимать с жидкостью, также имеющей кислый вкус. Например, гранулы можно добавлять к яблочному пюре, йогурту или фруктовому соку (яблочному, апельсиновому или ананасовому) с pH менее 5,5. Принцип дозирования гранул разработан с целью тщательного их перемешивания с кишечным содержимым, и лучшего распределения ферментов после их высвобождения внутри содержимого кишечника. Когда гранулы достигают тонкой кишки, кишечнорастворимая оболочка быстро разрушается и происходит высвобождение ферментов. Материалы и методы Для выполнения анализа влияния на бюджет был проведен литературный поиск с целью определения альтернативных препарату Креон® Микро лекарственных средств, которые могут использоваться в качестве заместительной терапии экзокринной недостаточности поджелудочной железы у детей с муковисцидозом. Поиск производился в библиографических базах данных MEDLINE (через интерфейс Pubmed), Google Scholar и российском индексе научного цитирования (РИНЦ, elibrary.ru). Одновременно с этим, из российского регистра больных с муковисцидозом были получены данные по половозрастному распределению и числу детей с муковисцидозом в Российской Федерации [7]. Далее была определена среднесуточная доза ферментных препаратов. При ее оценке опирались на следующее: при лечении муковисцидоза рекомендованные дозы составляют от 500 до 3000 ед. липазы на килограмм массы тела на прием пищи, но при этом не более 6-10 тысяч ед. липазы на килограмм в день у детей. Поскольку дети старше 4 лет обычно потребляют меньше жиров на килограмм массы тела, чем младшие дети, дозировка у них должна быть меньше (500 и 1000 ед. липазы на килограмм на прием пищи, соответственно [8]). Поскольку согласно имеющимся рекомендациям суточная доза составляет от 2 до 6 тыс. единиц липазы на килограмм массы тела [9], было предположено, что в среднем доза составляет 5000 единиц липазы на килограмм в сутки. Поправка на более низкую массу тела у детей с муковисцидозом не делалась [8], расчеты делались исходя из значений нормальной для данного возраста массы тела. Далее суточные дозы препаратов были умножены на число детей данной возрастной группы и стоимость липазной единицы. Для оценки стоимости ферментной терапии использовалась сумма всех стоимостей для детей в возрасте 12 лет. Предполагалось, что ферментные препараты получают 96,2% всех пациентов (согласно данным регистра [7]). Стоимость ферментных препаратов была взята как средняя стоимость препаратов в аптеках г. Санкт-Петербурга (pharmindex.ru, доступ осуществлен 27/02/2017). Кроме того, были проанализированы зарегистрированные цены ферментных препаратов в государственном реестре предельных отпускных цен (grls.rosminzdrav.ru). Были рассмотрены крайние случаи: – все пациенты получают препараты одной торговой марки, все пациенты получают препараты другой торговой марки, а также ситуацию, при которой используется комбинация препаратов. Предполагалось, что с 6 лет дети могут переходить на препараты, содержащие 25000 единиц липазы. Поскольку информации о долях рынка ферментных препаратов для лечения пациентов с муковисцидозом нет, но Креон® используется чаще всего, базовый анализ предполагал, что большая часть пациентов использует для заместительной терапии именно его. Результаты Препараты для заместительной терапии при экзокринной недостаточности поджелудочной железы известны давно. Они используются в заместительной терапии при недостаточности, вызванной такими заболеваниями, как муковисцидоз, хронический панкреатит и состояния после операций на поджелудочной железе. Длительное время рынок ферментных препаратов, содержащих сложные экстракты поджелудочной железы свиней или крупного рогатого скота (панкреатин, по американской терминологии) или более высокоактивные экстракты поджелудочной железы свиней (панкреолипаза1 Пакреолипаза содержит, согласно американской фармакопее в 12 раз больше липазы и в 4 раза больше протеазы и амилазы Поскольку было установлено, что для того, чтобы вместе с пищей пройти пилорический сфинктер размеры частиц ферментного препарата должны быть менее 2 мм [11,12], были разработаны микросферы и микротаблетки. Эти формы, значительно легче проходили вместе с химусом в двенадцатиперстную кишку и начинали раньше растворяться в кишечнике, чем способствовали лучшему перевариванию пищи. Это позволило пациентам с муковисцидозом перейти от ранее рекомендованной низкожировой, высокопротеиновой диеты к диете, содержащей значительное количество белков и жиров, что позволяло им получать достаточное количество энергии для потребностей организма. Дальнейшее развитие технологии микрокапсул позволило увеличить содержание липазы и оптимизировать дозировку. Вместе с тем, в 1990 году журнал JAMA [13] опубликовал клиническое наблюдение за пациентами с муковисцидозом, которым оригинальный препарат был заменен на воспроизведенный. Возникшая на этом фоне симптоматика со стороны желудочно-кишечного тракта и стеаторея были ликвидированы возвращением на оригинальный препарат. Анализ с использованием искусственного желудочного сока показал, что через час после контакта с ним в капсулах воспроизведенного препарата содержалось всего лишь 200 единиц липазы, тогда как в оригинальном препарате их содержание составляло 6820 единиц. Авторы сообщения указывали на явный дефект кишечнорастворимой оболочки воспроизведенных препаратов и призывали FDA принять меры. Интересно, что И.В. Маев и соавт. [14], сравнивая экономическую эффективность терапии препаратами Креон® и Мезим форте в эквивалентной дозе в Российской Федерации пришли к выводу, что первый приводит к сокращению сроков госпитализации на 7 суток, и это оборачивается экономией средств системы здравоохранения несмотря на большую стоимость препарата Креон®. Причиной снижения сроков госпитализации послужило то, что на фоне приема препарата Креон® быстрее происходило исчезновение болей и коррекция экзокринной панкреатической недостаточности. Как выяснилось, одной из причин большей эффективности препарата Креон® оказалось то, что измеренная активность протеаз в таблетке Мезим форте 10 000 оказалась значительно ниже (375 ЕД F.I.P.), чем в капсуле препарата Креон® 10 000 (600 ЕД F.I.P.). Иными словами, расхождения в номинальном содержании ферментов и их реальной концентрации наблюдаются в разных странах мира. Кроме того, поскольку панкреатические ферменты не являются стабильными, то производители часто увеличивали концентрацию ферментов (до 160% [15]) в сравнении с указанной на упаковке (overfill), для того, чтобы к концу срока годности препарата содержание ферментов находилось в пределах заявленной дозы [10, 16]. Связано это было с тем, что для препаратов панкреатических ферментов фармакопея включала нижнюю, но не верхнюю границу содержания ферментов. Постепенно пришло понимание того, что в фармакопее должны быть верхняя и нижняя граница для содержания ферментов, и FDA стало требовать, чтобы переполнения ферментами не было. В 2004 году FDA формально объявило, что панкреатические препараты для заместительной терапии должны проходить через стандартный процесс выхода на рынок (проходить клинические испытания), а для существующих производителей было дано 4 года возможности продавать препарат, не получая нового разрешения. Затем этот срок был продлен до 28 апреля 2010 года. Этот шаг FDA резко сократил число производителей на рынке США, которые имели право на введение препаратов панкреатических ферментов в гражданский оборот. Вместе с тем, отвечая на требования FDA, ряд компаний изменили состав и/или технологию изготовления панкреатических ферментов и провели клинические испытания новых формул. Одной из первых стала фирма Солвей, которая разработала новую формулу препарата Креон® (сейчас права на препарат принадлежат компании Эбботт Лэбораториз) и проверила ее эффективность и безопасность у пациентов с муковисцидозом в многоцентровом плацебо-контролируемом двойном слепом исследовании у детей 7-11 лет [17], а также в открытом многоцентровом исследовании без группы контроля у детей до 7 лет [18]. Эти исследования позволили FDA в 2009 году выдать первое разрешение на терапевтическое использование панкреатических ферментов в лечении муковисцидоза. В том же 2009 году разрешение на использование получил препарат Зенпеп (Zenpep®, Aptalis Pharma US, Inc. EUR-1008, также после проведения клинических испытаний в виде двойного слепого плацебо-контролируемого РКИ у детей старше 7 лет и дополнительного открытого исследования без группы контроля у детей младше 7 лет [19, 20]). Далее разрешения от FDA получили: в 2010 – Панкреаза (Pancreaze®, Janssen Pharmaceuticals, Inc.) и в 2012 – Ультреза (Ultresa™, Aptalis Pharma US, Inc.), Виоказа (Viokace™, Aptalis Pharma US, Inc.) и Пертзи (Pertzye®, Digestive Care, Inc.). За исключением препарата Пертзи, который содержит микросферы кишечного растворения с бикарбонатным буфером, и препарата Виоказа, который не покрыт кишечнорастворимой оболочкой, остальные разрешенные препараты представляют собой кишечнорастворимые капсулы, содержащие микросферы или микротаблетки. Как понятно из предшествующего обсуждения, для лечения пациентов с муковисцидозом единственно приемлемыми являются кишечнорастворимые капсулы с микросферами или микротаблетками, желательно те из них, для которых были проведены клинические испытания. В Российской Федерации в настоящий момент на рынке присутствует несколько препаратов, которые содержат микросферы и микротаблетки – это препараты Креон® (микросферы), Микразим® (пеллеты), Эрмиталь® (микротаблетки) и Пангрол® (микротаблетки). Первым из них на рынке появился препарат Креон®. Как отмечают Н. Ю. Каширская и соавт., включение в базисную терапию больных муковисцидозом современных микросферических заместительных ферментов привело к улучшению нутритивного статуса (массо-ростовой индекс (МРИ) увеличился с 89,8 до 93,8%), снижению количества больных со значительными нарушениями со стороны бронхолёгочной системы (с 45 до 38,1%), облегчению тяжести течения заболевания (количество больных с удовлетворительным течением заболевания по модифицированной шкале Швахмана–Брасфильда возросло с 44,4 до 48,5%). Наиболее значимое увеличение МРИ отмечалось в группе детей 3–6 лет. Авторы указывают, что произошедшее в 1993-2003 годах увеличение продолжительности жизни с 16 до 27,9 лет связано, в первую очередь, с введением в 1993 г. в терапию микросферических панкреатических ферментов [21]. С другой стороны, проведенное мультицентровое исследование клинической эффективности и безопасности препарата Микразим® у 42 детей больных муковисцидозом выявило, что он дает высокий процент (26%) серьезных побочных явлений со стороны желудочно-кишечного тракта, потребовавших его отмены, и еще у 14% пациентов отсутствовала эффективность. В связи с этим он не был рекомендован к широкому применению у больных муковисцидозом [22]. В 2016 году А. В. Орлов и соавт. [23] опубликовали данные оценки эффективности и безопасности препарата Пангрол® у пациентов с муковисцидозом. Хотя объективно авторы установили отсутствие выраженных различий в эффективности и безопасности препарата, врачи и пациенты оценивали эффективность и переносимость препарата Пангрол® достоверно ниже, чем препарата Креон®. Соответственно, кроме препарата Креон® по результатам российских клинических испытаний для лечения больных муковисцидозом мог быть рекомендован дополнительно только препарат Эрмиталь® [9], хотя А. В. Орлов и соавт. [23] считают препарат Пангрол® альтернативой препарату Креон®. В 2015 году Н.Ю. Каширская и соавт. [6] опубликовали результаты трехмесячного открытого многоцентрового клинического испытания препарата Креон® Микро, проведенного в Российской Федерации. В него были включены дети в возрасте от одного месяца до 4 лет. В результате было показано улучшение нутритивного статуса детей на фоне приема данного препарата, а 95% родителей отметили "простоту" применения препарата. Соответственно, альтернативой в лечении экзокринной недостаточности поджелудочной железы в Российской Федерации препарату Креон® Микро являются препараты Креон®, Пангрол® и Эрмиталь®. В табл. 1 приведены данные о сравнительной стоимости 1000 липазных единиц по аптечным данным и данным регистра предельных отпускных цен препаратов Креон®, Пангрол® и Эрмиталь®. Таблица 1. Сравнительный анализ стоимости единицы ферментных препаратов, рублей за 1000 липазных единиц. 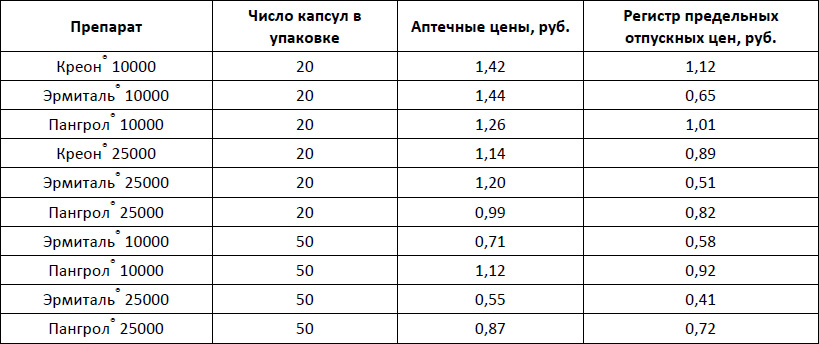 Как видно из табл. 1, стоимости препаратов Креон® и Эрмиталь® в регистре предельных отпускных цен отличались почти в два раза, а аптечные цены вели себя несколько иначе. Сравнение цены Креон® 10000, Пангрол® 10000 и Эрмиталь® 10000 показывает, что цены отличаются в зависимости от количества капсул в упаковке. В большой упаковке стоимость 1000 липазных единиц при использовании препарата Эрмиталь® оказывалась в два раза ниже, чем стоимость препарата Креон® 10000, а вот если использовались сравнимые упаковки, то цена препарата Эрмиталь® была даже выше, чем препарата Креон®. Стоимость препарата Пангрол® в сравниваемых упаковках была ниже, а в больших упаковках превышала стоимость препарата Эрмиталь®. Поскольку ферментные препараты закупаются в основном в амбулаторной сети, то необходимо больше ориентироваться на соотношение цен в аптечном сегменте, хотя это и приводит к очевидной проблеме некоторого различия аптечных цен в разных регионах. Согласно методике регулирования цен на препараты, входящие в список ЖНВЛП, регистрационная стоимость препарата Креон® Микро за одну липазную единицу будет соответствовать таковой у Креон® 10000, составляя 1,12 рублей за 1000 липазных единиц. Соответственно, ожидать значительных изменений в уровне расходов при применении препарата Креон® Микро вместо препарата Креон® не предполагается. Проведенные расчеты показывают, что, если все пациенты в возрасте до 12 лет (всего их, по данным регистра, 1820 человек [7]) принимают Креон® 10000 или Креон® Микро, расходы бюджета на приобретение ферментых препаратов составляют 99,3 млн. рублей. Если, при этом, дети старше 6 лет начинают принимать Креон® 25000, то оценка расходов снижается до 85,8 млн. рублей. Данные по проникновению препаратов Эрмиталь® и Пангрол® на рынок средств заместительной терапии панкреатической недостаточности при муковисцидозе в доступной литературе нам найти не удалось. Однако, учитывая, что специалисты рекомендовали Эрмиталь® как препарат второй линии [22], не приходится сомневаться в том, что его присутствие на рынке не является значительным. Более того, как отмечалось в работе А.В. Орлова и соавт. [23], большинство врачей и пациентов в их исследовании предпочитали остаться на терапии препаратом Креон®, вместо того, чтобы заменять его на Пангрол®. Поскольку стоимость препарата Пангрол® в большой упаковке (50 капсул) превышает таковую для препарата Эрмиталь®, в дальнейших расчетах возможность значительного проникновения этого препарата на рынок ферментных средств для лечения муковисцидоза не рассматривалась, поскольку даже если бы это произошло, снижение расходов было бы меньшим, чем от значительного проникновения препарата Эрмиталь®. Поэтому мы повторили расчеты, приняв, что до 30% пациентов старше 6 лет будут вместо Креон® 25000 принимать Эрмиталь® 25000 (50 капсул в упаковке). В этой ситуации оценка расходов снижается до 77,5 млн. рублей в год на всех страдающих муковисцидозом пациентов в возрасте до 12 лет. Если же треть пациентов вместо препарата Эрмиталь® принимают препарат Пангрол® 25000 (50 капсул в упаковке), то в этом случае (20% пациентов старше 6 лет принимают Эрмиталь®, 10% – Пангрол®) расходы увеличиваются на 1,5 млн. рублей – до 79 млн. рублей в год на всех пациентов с муковисцидозом в возрасте до 12 лет. Таким образом на бюджет влияет, в основном, степень проникновения на рынок препарата Эрмиталь®. Еще одним предполагаемым эффектом от внесения Креон® Микро в список ЖНВЛП является возможное сокращение потребности в капсулах с ферментным препаратом, в особенности у детей младшего возраста. В настоящее время для применения у детей младшего возраста, которые не могут проглотить капсулу, рекомендуется вскрыть ее и отобрать необходимое количество микрогранул. Например, чтобы получить дозировку в 5000 липазных единиц, необходимо вскрыть капсулу, разделить содержимое на две части, одну принять, другую оставить на следующий раз. Очевидно, что такой подход может приводить к появлению отходов и неточному дозированию. По этой причине мы повторили расчеты расходов на терапию, округлив дозировки вначале до ближайших 10000 единиц в каждой возрастной группе в возрасте до 6 лет, предполагая, что вскрытые капсулы не сохраняются (предположение разумно при оплате терапии государством). Суммарные расходы выросли на 1,5 млн. рублей в год (табл. 2). Далее было сделано предположение, что около 10% пациентов вместо препарата Эрмиталь® 25000 в возрасте старше 6 лет принимают Пангрол® 25000. В этой ситуации расходы увеличиваются на 3 млн. рублей в год. Соответственно, за счет отходов стоимость терапии может быть на 1,5-3,0 млн. рублей в год выше, чем при игнорировании возможных отходов. Использование более точного дозирования при применении Креон® Микро может привести к экономии около 1,5-3,0 млн. рублей в год. Таблица 2. Предполагаемые расходы на терапию экзокринной недостаточности поджелудочной железы у детей с муковисцидозом в возрасте до 12 лет в Российской Федерации (детали в тексте).  Выводы Согласно литературным данным, включение в базисную терапию больных муковисцидозом современных микросферических заместительных ферментов приводит к улучшению нутритивного статуса и снижению количества больных со значительными нарушениями со стороны бронхолёгочной системы. Родители, согласно данным российского клинического испытания препарата Креон® Микро, в 95% случаев отмечают "простоту" применения препарата. Проведенный анализ позволяет предположить, что введение в практику препарата Креон® Микро не приведет к изменению расходов бюджета Российской Федерации, которые будут сильно зависеть от соотношения частоты использования капсул Креон® 25000 и Креон® 10000, а также степени проникновения на рынок препарата Эрмиталь®, в особенности с большим числом капсул в упаковке. С другой стороны, устранение возможных потерь после вскрытия капсул Креон® 10000 или Креон® 25000 (хранение вскрытой капсулы не более суток) может привести к экономии средств бюджета в объеме, как минимум, 1,5-3,0 млн. рублей. Также был выполнен анализ возможных предотвращенных потерь в группе детей в возрасте до 2 лет. В анализе исходили из того, что в условиях отсутствия препарата Креон® Микро вторая половина капсулы Креон® 10000 будет утилизироваться, соответственно доза Креон® 10000 в сутки будет равна частоте приема пищи умноженной на среднюю дозу на прием пищи, округленную до ближайших 10000 липазных единиц (в отличие от других сценариев, где учитывалась только суточная доза). Расчеты показывают, что в таких условиях (отказ от хранения вскрытой капсулы), в данной группе будет происходить сокращение расходов с 8,98 млн. рублей в год до 5,91 млн. рублей в год или на 34,2%. Соответственно, замена Креон® 10000 на Креон® Микро приводит к экономии бюджета за счет снижения потерь при дозировании на 34,2%. Список литературы 1. van Gool K., Norman R., Delatycki M. B. et al. Understanding the costs of care for cystic fibrosis: an analysis by age and health state // Value Health. – 2013. – Vol. 16. – № 2. – P. 345–355. 2. Mlcoch T., Klimes J., Fila L. et al. Cost-of-illness analysis and regression modeling in cystic fibrosis: a retrospective prevalence-based study // Eur J Health Econ. – 2016. – Vol. 18. – № 1. – P. 73–82. 3. Heimeshoff M., Hollmeyer H., Schreyogg J. et al. Cost of illness of cystic fibrosis in Germany: results from a large cystic fibrosis centre // Pharmacoeconomics. – 2012. – Vol. 30. – № 9. – P. 763–777. 4. Colombo C., Dacco V., Alicandro G. et al. Cost of cystic fibrosis: analysis of treatment costs in a specialized center in northern Italy // Adv Ther. – 2013. – Vol. 30. – № 2. – P. 165–175. 5. Steinkamp G. Relationship between nutritional status and lung function in cystic fibrosis: cross sectional and longitudinal analyses from the German CF quality assurance (CFQA) project // Thorax. – 2002. – Vol. 57. – № 7. – P. 596–601. 6. Kashirskaya N.Y., Kapranov N.I., Sander-Struckmeier S., Kovalev V. Safety and efficacy of Creon micro in children with exocrine pancreatic insufficiency due to cystic fibrosis // J. Cyst. Fibros. – 2015. – Vol. 14. – № 2. – P. 275–281. 7. Регистр больных муковисцидозом в Российской Федерации. 2015 год. / Под ред. Е.И. Кондратьевой, С.А. Красовского, А.Ю. Воронковой и др. – Москва: Медпрактика-М, 2016. – С. 72. 8. Gardner T.B., Munson J.C., Morden N.E. The FDA and prescription pancreatic enzyme product cost // Am. J. Gastroenterol. – 2014. – Vol. 109. – № 5. – P. 624–625. 9. Каширская Н.Ю., Капранов Н.И. Опыт терапии экзокринной недостаточности поджелудочной железы при муковисцидозе в России // РМЖ. – 2011. – Т. 19. – № 12. – С. 737–741. 10. Kraisinger M., Hochhaus G., Stecenko A. et al. Clinical pharmacology of pancreatic enzymes in patients with cystic fibrosis and in vitro performance of microencapsulated formulations // J Clin Pharmacol. – 1994. – Vol. 34. – № 2. – P. 158–166. 11. Kuhnelt P., Mundlos S., Adler G. Einfluss der Pelletgroesse eines Pankreasenzympraeparates auf die duodenale lipolytische Aktivitaet // Z Gastroenterol. – 1991. – Vol. 29. – P. 417–421. 12. Mossner J., Keim V. Therapie mit Pankreasenzymen // Dtsch Arztebl Int. – 2011. – № 34-35. – P. 578–582. 13. Hendeles L., Dorf A., Stecenko A., Weinberger M. Treatment failure after substitution of generic pancrelipase capsules. Correlation with in vitro lipase activity // JAMA. – 1990. – Vol. 263. – № 18. – P. 2459–2461. 14. Маев И.В., Кучерявый Ю.А., Трошина И.В. и др. Фармакоэкономические показатели заместительной ферментной терапии экзокринной панкреатической недостаточности // Клинические перспективы гастроэнтерологии, гепатологии. – 2011. – № 4. – С. 18–25. 15. Taylor C. J., Thieroff-Ekerdt R., Shiff S. et al. Comparison of two pancreatic enzyme products for exocrine insufficiency in patients with cystic fibrosis // J. Cyst. Fibros. – 2016. – Vol. 15. – № 5. – P. 675–680. 16. Kuhn R.J., Eyting S., Henniges F., Potthoff A. In Vitro Comparison of Physical Parameters, Enzyme Activity, Acid Resistance, and pH Dissolution Characteristics of Enteric-Coated Pancreatic Enzyme Preparations: Implications for Clinical Variability and Pharmacy Substitution // J Pediatr Pharmacol Ther. – 2007. – Vol. 12. – № 2. – P. 115–128. 17. Graff G.R., Maguiness K., McNamara J. et al. Efficacy and tolerability of a new formulation of pancrelipase delayed-release capsules in children aged 7 to 11 years with exocrine pancreatic insufficiency and cystic fibrosis: a multicenter, randomized, double-blind, placebo-controlled, two-period crossover, superiority study // Clin Ther. – 2010. – Vol. 32. – № 1. – P. 89–103. 18. Graff G.R., McNamara J., Royall J. et al. Safety and tolerability of a new formulation of pancrelipase delayed-release capsules (CREON) in children under seven years of age with exocrine pancreatic insufficiency due to cystic fibrosis: an open-label, multicentre, single-treatment-arm study // Clin Drug Investig. – 2010. – Vol. 30. – № 6. – P. 351–364. 19. Wooldridge J.L., Heubi J.E., Amaro-Galvez R. et al. EUR-1008 pancreatic enzyme replacement is safe and effective in patients with cystic fibrosis and pancreatic insufficiency // J. Cyst. Fibros. – 2009. – Vol. 8. – № 6. – P. 405–417. 20. Toskes P.P., Secci A., Thieroff-Ekerdt R. et al. Efficacy of a novel pancreatic enzyme product, EUR-1008 (Zenpep), in patients with exocrine pancreatic insufficiency due to chronic pancreatitis // Pancreas. – 2011. – Vol. 40. – № 3. – P. 376–382. 21. Каширская Н.Ю., Капранов Н.И., Васильева Ю.И. Фармакоэкономическая эффективность некоторых современных методов терапии у детей с муковисцидозом // Педиатрическая фармакология. – 2006. – Т. 3. – № 3. – С. 32–37. 22. Ашерова И.К., Каширская Н.Ю., Капранов Н.И. Сравнение эффективности и безопасности препаратов Эрмиталь и Креон в эквивалентных дозах у больных муковисцидозом с недостаточностью экзокринной функции поджелудочной железы // Вестник новых медицинских технологий. – 2012. – Т. XIX. – № 2. – С. 94–96. 23. Орлов А.В., Никитина М.И., Пашкевич А.А., Ковалев В.Н. Эффективность и безопасность мини-таблетированного панкреатина Пангрол 10 000 ед и 25 000 ед у больных с муковисцидозом // Педиатр. – 2016. – Т. VII. – № 1. – С. 22–26.
Date of publication 15/04/2017. Abstract The article considers the problem of choosing the most appropriate drugs for replacement therapy of endocrine pancreatic insufficiency. The possible consequences for the budget of the Russian Federation of including in the VED lists a new drug for substitution therapy, Creon® Micro, are assessed. Authors conclude that the widespread use of this drug will provide for significant budget savings while maintaining the effectiveness of treatment. Key words Cystic Fibrosis, Enzyme Therapy, Creon® Micro, pancreatic enzymes, enteric-cleavage capsules References 1. Gool, Kees Van, Richard Norman, Martin B. Delatycki, Jane Hall, and John Massie. "Understanding the Costs of Care for Cystic Fibrosis: An Analysis by Age and Health State." Value in Health 16, no. 2 (2013): 345-55. doi:10.1016/j.jval.2012.12.003. 2. Mlčoch, Tomáš, Jiří Klimeš, Libor Fila, Věra Vávrová, Veronika Skalická, Marek Turnovec, Veronika Krulišová, Jitka Jirčíková, Dana Zemková, Klára Vilimovská Dědečková, Alena Bílková, Vladimíra Frühaufová, Lukáš Homola, Zuzana Friedmannová, Radovan Drnek, Pavel Dřevínek, Tomáš Doležal, and Milan Macek. "Cost-of-illness analysis and regression modeling in cystic fibrosis: a retrospective prevalence-based study." The European Journal of Health Economics 18, no. 1 (2016): 73-82. doi:10.1007/s10198-015-0759-9. 3. Heimeshoff, Mareike, Helge Hollmeyer, Jonas Schreyögg, Oliver Tiemann, and Doris Staab. "Cost of Illness of Cystic Fibrosis in Germany." PharmacoEconomics 30, no. 9 (2012): 763-77. doi:10.2165/11588870-000000000-00000. 4. Colombo, Carla, Valeria Daccò, Gianfranco Alicandro, Silvana Loi, Silvio Mazzi, Carlo Lucioni, and Roberto Ravasio. "Cost of Cystic Fibrosis: Analysis of Treatment Costs in a Specialized Center in Northern Italy." Advances in Therapy 30, no. 2 (2013): 165-75. doi:10.1007/s12325-013-0008-5. 5. Steinkamp, G. "Relationship between nutritional status and lung function in cystic fibrosis: cross sectional and longitudinal analyses from the German CF quality assurance (CFQA) project." Thorax 57, no. 7 (2002): 596-601. doi:10.1136/thorax.57.7.596. 6. Kashirskaya, Nataliya Y., Nikolay I. Kapranov, Suntje Sander-Struckmeier, and Vladimir Kovalev. "Safety and efficacy of Creon® Micro in children with exocrine pancreatic insufficiency due to cystic fibrosis." Journal of Cystic Fibrosis 14, no. 2 (2015): 275-81. doi:10.1016/j.jcf.2014.07.006. 7. The register of patients with cystic fibrosis in the Russian Federation for the year 2015. Edited by E. I. Kondrateva, S. A. Krasovskij, A. Ju Voronkova et al. Moscow: Medpraktika-M, 2016. 8. Gardner, Timothy B., Jeffrey C. Munson, and Nancy E. Morden. "The FDA and Prescription Pancreatic Enzyme Product Cost." The American Journal of Gastroenterology 109, no. 5 (2014): 624-25. doi:10.1038/ajg.2013.430. 9. Kashirskaya, A. Yu, and N. I. Kapranov. "Experience of therapy of exocrine pancreatic insufficiency in cystic fibrosis in Russia." Rossijskij medicinskij zhurnal 19, no. 12 (2011): 737-41. 10. Kraisinger, Marijo, Guenther Hochhaus, Arlene Stecenko, Ellen Bowser, and Leslie Hendeles. "Clinical Pharmacology of Pancreatic Enzymes in Patients with Cystic Fibrosis andIn VitroPerformance of Microencapsulated Formulations." The Journal of Clinical Pharmacology 34, no. 2 (1994): 158-66. doi:10.1002/j.1552-4604.1994.tb03981.x. 11. Kuhnelt P., Mundlos S., Adler G. "Einfluss der Pelletgroesse eines Pankreasenzympraeparates auf die duodenale lipolytische Aktivitaet" Zeitschrift für Gastroenterologie Vol. 29 (1991): 417-21. 12. Mossner J., Keim V. "Therapie mit Pankreasenzymen." Deutsches Ärzteblatt International no. 34-35 (2011): 578–82. 13. Hendeles, Leslie. "Treatment Failure After Substitution of Generic Pancrelipase Capsules." Jama 263, no. 18 (1990): 2459. doi:10.1001/jama.1990.03440180065033. 14. Maev, I. V., Yu A. Kucheryavyj, and I. V. Troshina. "Pharmacoeconomic indicators of substitution enzyme therapy of exocrine pancreatic insufficiency." Klinicheskie perspektivy gastroehnterologii, gepatologii, no. 4 (2011): 18-25. 15. Taylor, C.j., R. Thieroff-Ekerdt, S. Shiff, L. Magnus, R. Fleming, and C. Gommoll. "Comparison of two pancreatic enzyme products for exocrine insufficiency in patients with cystic fibrosis." Journal of Cystic Fibrosis 15, no. 5 (2016): 675-80. doi:10.1016/j.jcf.2016.02.010. 16. Kuhn R.J., Eyting S., Henniges F., Potthoff A. "In Vitro Comparison of Physical Parameters, Enzyme Activity, Acid Resistance, and pH Dissolution Characteristics of Enteric-Coated Pancreatic Enzyme Preparations: Implications for Clinical Variability and Pharmacy Substitution." J Pediatr Pharmacol Ther. 2007 Apr;12(2):115-28. doi: 10.5863/1551-6776-12.2.115. 17. Graff G.R., Maguiness K., McNamara J. et al. "Efficacy and tolerability of a new formulation of pancrelipase delayed-release capsules in children aged 7 to 11 years with exocrine pancreatic insufficiency and cystic fibrosis: a multicenter, randomized, double-blind, placebo-controlled, two-period crossover, superiority study." Clin Ther. 2010 Jan;32(1):89-103. doi: 10.1016/j.clinthera.2010.01.012. 18. Graff, Gavin R., John Mcnamara, James Royall, Steven Caras, and Kristin Forssmann. "Safety and Tolerability of a New Formulation of Pancrelipase Delayed-Release Capsules (CREON®) in Children Under Seven Years of Age with Exocrine Pancreatic Insufficiency due to Cystic Fibrosis." Clinical Drug Investigation 30, no. 6 (2010): 351-64. doi:10.2165/11533390-000000000-00000. 19. Wooldridge, Jamie L., James E. Heubi, Rodolfo Amaro-Galvez, Steven R. Boas, Kathryn V. Blake, Samya Z. Nasr, Barbara Chatfield, Susanna A. Mccolley, Marlyn S. Woo, Karen A. Hardy, Richard M. Kravitz, Cristina Straforini, Marco Anelli, and Candace Lee. "EUR-1008 pancreatic enzyme replacement is safe and effective in patients with cystic fibrosis and pancreatic insufficiency." Journal of Cystic Fibrosis 8, no. 6 (2009): 405-17. doi:10.1016/j.jcf.2009.07.006. 20. Toskes, Phillip P., Angelo Secci, and Ruth Thieroff-Ekerdt. "Efficacy of a Novel Pancreatic Enzyme Product, EUR-1008 (Zenpep), in Patients With Exocrine Pancreatic Insufficiency Due to Chronic Pancreatitis." Pancreas 40, no. 3 (2011): 376-82. doi:10.1097/mpa.0b013e31820b971c. 21. Kashirskaya, N. Yu, N. I. Kapranov, and Yu I. Vasileva. "Pharmacoeconomic efficiency of some modern therapy methods in children with cystic fibrosis." Pediatricheskaya farmakologiya 3, no. 3 (2006): 32-37. 22. Asherova, I. K., N. Yu Kashirskaya, and N. I. Kapranov. "Comparison of efficacy and safety of Ermytal and Creon preparations in equivalent doses in patients with cystic fibrosis with insufficient exocrine pancreatic function." Vestnik novyh medicinskih tekhnologij XIX, no. 2 (2012): 94-96. 23. Orlov, A. V., M. I. Nikitina, A. A. Nikitina, and V. N. Kovalev. "Efficacy and safety of the mini-tablet pancreatin Pangrol 10 000 units and 25 000 units in patients with cystic fibrosis." Pediatr VII, no. 1 (2016): 22-26. |
[ См. также ] Рубрики |
|||||
|
|
|
Журнал «Медицина» © ООО "Инновационные социальные проекты"
|