| О журнале | Редколлегия | Редсовет | Архив номеров | Поиск | Авторам | Рецензентам | English |
Создание и валидация способа количественного определения бисопролола в новой фармакологической композиции "Бисопролозоль"
Автор для корреспонденции: Кобелева Татьяна Алексеевна; e-mail: kobeleva@tyumsmu.ru. Финансирование. Исследование не имело спонсорской поддержки. Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов. Аннотация Введение. При разработке новых фармакологически активных композиций и их внедрении в экстемпоральное изготовление и промышленное производство обязательным разделом является всестороннее исследование свойств лекарственного препарата с применением современных методов анализа, сочетающих высокие метрологические характеристики, экспрессность, чувствительность, точность, доступность, надежность. Разработка аналитических методик контроля качества новых лекарственных композиций является актуальной задачей современного фармацевтического анализа. Цель исследования – разработка и валидация способа количественного определения бисопролола в новой фармакологической композиции "Бисопролозоль". Материал и методы исследования. Для осуществления анализа использовали фармацевтическую субстанцию бисопролола фумарата, глицериновый гидрофильный гель "Тизоль", мазь "Бисопролозоль", состоящую из 0,5 % селективного бета-блокатора в титансодержащем глицерогидрогеле. В ходе эксперимента применены спектрофотометр СФ-2000 отечественного производства и метод абсорбционной спектрофотометрии в ультрафиолетовой области. В программе Microsoft Office Excel 2016, используя метод регрессионного анализа, выполняли статистическую обработку полученных данных (ОФС.1.1.0013.15 "Статистическая обработка результатов химического эксперимента"). Методика оценена по валидационным параметрам: специфичность, линейность, правильность и прецизионность. Результаты исследования. В ходе изучения электронных спектральных кривых бисопролола определили, что анализ его рационально осуществлять при длине волны 274 нм (экспериментально определенный максимум поглощения). В процессе проведения исследования установили чувствительность определения лекарственного средства, которая равна 5,260 мкг/мл при A(min) = 0,02. Результаты количественного анализа бисопролола в фармакологической композиции "Бисопролозоль" показали, что масса селективного блокатора адренергических рецепторов (0,0409-0,0536 г) находится в допустимых пределах согласно нормативной документации для мягких лекарственных форм (Приказ Министерства здравоохранения Российской Федерации № 751н от 26.10.2015 г.). Заключение. В рамках настоящего эксперимента выбраны оптимальные условия реализации спектрофотометрического метода анализа, на основании чего разработан, валидирован и представлен способ количественного определения бисопролола в новой фармакологической композиции "Бисопролозоль" с погрешностью, не превышающей ± 1,89 %. Ключевые слова бисопролол, гель "Тизоль", спектрофотометрия, валидация, количественное определение doi: 10.29234/2308-9113-2022-10-2-25-33 Для цитирования: Кобелева Т. А., Сичко А. И., Попова М. И. Создание и валидация способа количественного определения бисопролола в новой фармакологической композиции "Бисопролозоль". Медицина 2022; 10(2): 25-33. Введение В последнее время бета-адреноблокаторы, известные как препараты, оказывающие гипотензивный, антиаритмический и антиангинальный эффекты, стали основной формой лечения инфантильных гемангиом – самых распространенных сосудистых опухолей детского возраста [5,6]. Учеными Уральского государственного медицинского университета были разработаны фармакологические композиции бета-блокаторов в смеси с гидрофильным коагуляционным гелем "Тизоль". Аквакомплекс глицеросольвата титана используется в качестве проводника лекарственных средств при наружном применении, что повышает активность локальной терапии вследствие увеличения глубины проникновения доставляемого фармакологически активного вещества до патологического участка [2]. Сочетанная комбинация селективного блокатора бета-1-адренорецепторов бисопролола и геля "Тизоль" может быть рекомендована в качестве аппликационного лекарственного препарата в лечении гиперплазии сосудов у детей. Для нового лекарственного средства, внедряемого в медицинскую практику, должна разрабатываться нормативная документация, включающая в себя методики по установлению качества его изготовления. Цель работы Цель работы – разработка и валидация способа количественного определения бисопролола в новой фармакологической композиции "Бисопролозоль". Материал и методы исследования Для осуществления анализа использовали фармацевтическую субстанцию бисопролола фумарата (Ипка Лабораториз Лимитед, Индия, ФС-001472), гель "Тизоль" (ООО "Олимп", Россия, г. Екатеринбург, ФСП-3157-06), спирт этиловый (ООО "Гиппократ", Россия, г. Самара, ФС.2.1.0036.15), кислоту хлористоводородную – стандарт-титр с С = 0,1 моль/дм3 (АО "НПИП "Уралхиминвест", Россия, г. Уфа, ТУ 2642-001-33813273-97), мазь "Бисопролозоль", представляющую собой сочетанную комбинацию 0,05 г селективного бета-блокатора и титансодержащего аквагеля до 10,0 г. В процессе эксперимента применен спектрофотометр СФ-2000 (ЗАО "ОКБ СПЕКТР", Россия, г. Санкт-Петербург) и фармакопейный метод спектрофотометрии в УФ-области, используемый для качественного анализа бисопролола фумарата [1,3]. Статистическую обработку полученных экспериментальных данных проводили на основе метода регрессионного анализа в программе Microsoft Office Excel 2016. Валидационную оценку разработанной методики выполняли по следующим показателям: специфичность, линейность, правильность и прецизионность. При анализе бисопролола в модельной лекарственной форме (0,05 г бета-блокатора в 10 мл этилового спирта) в мерную колбу объемом 25 мл (V(общ)) вносили 1,0 мл исследуемого спиртового раствора (V) и доводили объем раствора в колбе до метки этанолом. Затем к 5 мл полученной смеси (V(п)) приливали этиловый спирт до общего объема 10 мл (V1) и с помощью спектрофотометра проводили измерение оптической плотности раствора при λ = 274 нм. По полученным значениям опытов и рассчитанному уравнению градуировочной зависимости (А = 0,0038∙C) находили содержание препарата (С(бис), мкг/мл) и рассчитывали массу бисопролола в лекарственной форме (1): m (бис)= ( С(бис)*V(общ)*V1*10 ) / ( 106*V*V(п) ) В ходе количественного определения бисопролола в лекарственной композиции "Бисопролозоль", к точной навеске мази (около 0,5 г) приливали 2,0 мл 0,01 моль/л раствора хлористоводородной кислоты и спирт этиловый до общего объема 10 мл, смесь фильтровали, используя обеззоленный фильтр марки ФМ. К 2,0 мл фильтрата добавляли 3,0 мл этанола и измеряли оптическую плотность раствора при длине волны 274 нм с помощью СФ-2000. Раствором сравнения служила этанольная вытяжка из мазевой основы, приготовленная аналогично методике количественного определения бисопролола в сочетанной комбинации с гелем "Тизоль". По уравнению градуировочной кривой находили концентрацию селективного бета-блокатора в пробе (С(бис), мкг/мл), а по формуле 2 вычисляли его массу в мази (2): m (бис)= ( С(бис)*V(общ)*V2*P ) / ( 106*a(мази)*V1 ) Где, а(мази) – точная навеска мази, взятая для анализа, г; Р – масса мягкой лекарственной формы, г; V1, V2 – коэффициент разбавления (2 мл и 5 мл, соответственно); V(общ) – объем смеси, в которой растворена навеска мази (10 мл). Результаты и обсуждение Для разработки методики определения содержания бисопролола в мази "Бисопролозоль" изучили ультрафиолетовые спектры поглощения бета-блокатора в этаноле (рис. 1, кривая 4). Рис. 1. Спектральные кривые бисопролола, геля "Тизоль" и этанола: 1 – этанольный раствор геля "Тизоль" 4,0∙10-5 моль/л; 2 – этанол; 3 – этанольная вытяжка бисопролола из мази 1·10-4 моль/л; 4 – этанольный раствор бисопролола 2,0·10-4 моль/л; 5 – этанольный раствор бисопролола 1,0·10-4 моль/л и геля "Тизоль" 1,0·10-4 моль/л 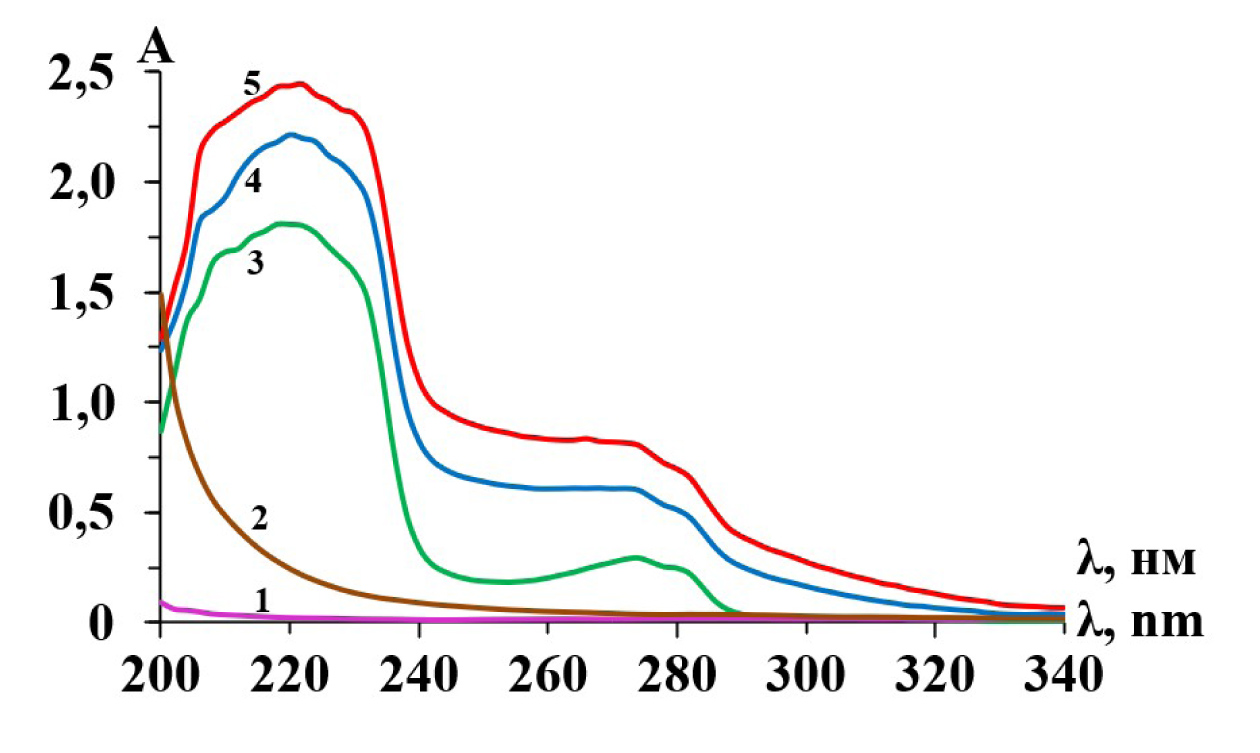 В результате проведенных опытов установлено, что спектральная кривая бисопролола в смеси с гелем "Тизоль" (рис. 1, кривая 5) имеет аналогичные значения положений экстремумов, как и в случае отсутствия мазевой основы (рис. 1, кривая 4). Кроме того, спектр поглощения этанольной вытяжки лекарственного средства из мази (рис.1, кривая 3) имеет одинаковую форму с такими же экстремальными полосами. Для количественного анализа бисопролола использовали этанольную вытяжку из мягкой лекарственной формы и дальнейшие исследования проводили при втором максимуме (λ = 274 нм). Гель "Тизоль" и этанол практически не поглощает свет в данной области. Таким образом, мазевая основа, частично перешедшая в спиртовую среду, не оказывает значительного влияния на анализ селективного блокатора адренорецепторов. Провели валидацию методики количественного определения бисопролола по показателям специфичности, линейности, правильности и прецизионности [4]. Чувствительность анализа рассчитывали через предел обнаружения в мкг/мл с учетом градуировочного коэффициента. В таблице 1 приведены результаты расчетов. Специфичность. С целью определения специфичности снимали спектры поглощения спирта этилового и раствора геля "Тизоль" в этаноле. Полученные электронные спектры "плацебо" не включали в себя пики, характерные для растворов лекарственного средства (рис. 1, кривые 1 и 2). Линейность. Для оценки линейности методики ставили шесть дублирующих опытов, в ходе которых проводили измерение оптических плотностей растворов бисопролола в пределах концентраций 20,0–120,0 мкг/мл. Вычисляли показатели линейной регрессии (табл. 1). Таблица 1. Анализ линейности методики.
Установили, что свободный член линейного уравнения статистически незначим (табл. 2). Линейность считали оптимальной при показателях коэффициента корреляционной зависимости |r| ≥ 0,99. Таблица 2. Уравнение линейной зависимости.
Рис. 2. Калибровочная модель зависимости оптической плотности от концентрации раствора бисопролола фумарата. 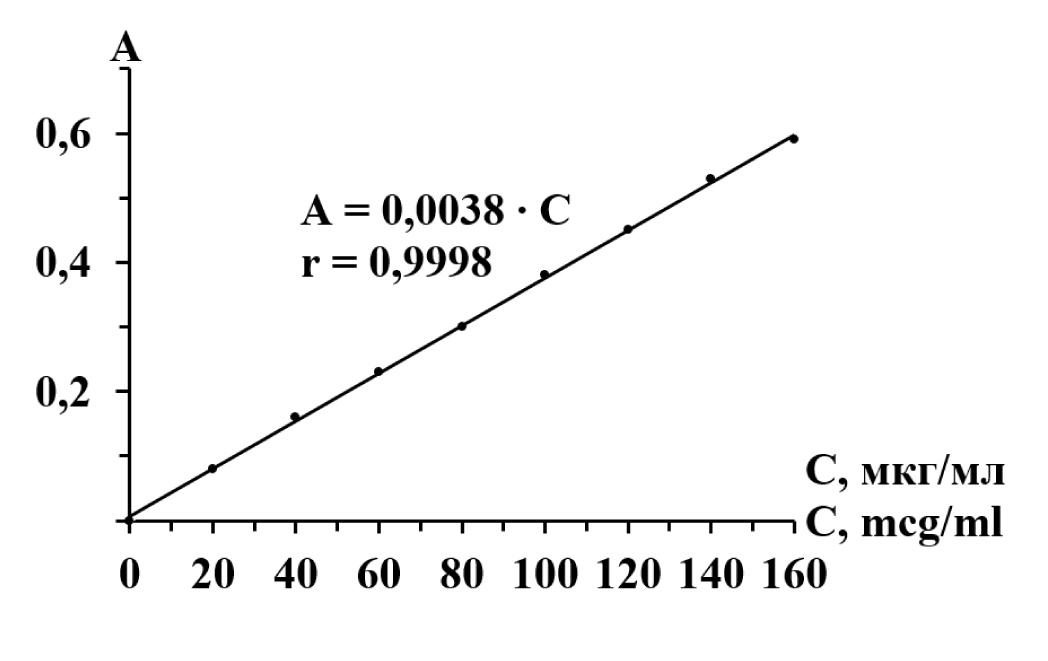 Построение графика производили на основании данных Таблицы 1. Представленная на рис. 2 прямая характеризует линейную зависимость между концентрацией бисопролола и оптической плотностью. Это указывает на подчинение растворов основному закону поглощения света в области концентраций лекарственного препарата 10,0 – 160,0 мкг/мл, что позволяет осуществлять количественное определение его в мази спектрофотометрическим методом. Правильность и прецизионность. Повторяемость (сходимость) валидируемой методики оценивали в короткий промежуток времени в одинаковых регламентированных условиях одной химической лаборатории, используя эталонные смеси бисопролола, по данным восьми параллельных опытов. Внутрилабораторную прецизионность определяли с участием двух провизоров-аналитиков в разные дни. Установили, что ошибка анализа не превышает ± 1,89 % (табл. 3). Таблица 3. Результаты оценки правильности и прецизионности методики анализа бисопролола методом спектрофотометрии.
Найденные значения стандартного отклонения (прецизионность) и относительной ошибки анализа (правильность) не выходят за границу 100±2,0%. Аналитическая область. Диапазон концентраций бисопролола, в пределах которого доказаны приемлемые линейность, прецизионность, правильность методики имеет значения 10,0 – 160,0 мкг/мл. В процессе исследования апробировали методику спектрофотометрического определения содержания бисопролола в модельной смеси и лекарственном препарате "Бисопролозоль" с применением расчетного способа по уравнению градуировочного графика. В табл. 4 и 5 представлены результаты количественного анализа лекарственного средства. Таблица 4. Данные анализа бисопролола в модельной смеси.
Таблица 5. Данные анализа бисопролола в фармакологической композиции "Бисопролозоль".
По результатам проведенных опытов установлено, что содержание бисопролола в модельной смеси (табл. 4) имеет значения в диапазоне от 0,0481 г до 0,0518 г при допустимой норме отклонений 0,040 – 0,060 г (Приказ Минздрава России № 751н). Согласно экспериментальным данным, найденная масса лекарственного средства в мази "Бисопролозоль" имеет значения 0,0409 – 0,0536 г (табл. 5) и находится в пределах, допустимых по нормативной документации для мягких лекарственных форм. Заключение Таким образом, в ходе настоящего эксперимента установлена чувствительность анализа бисопролола и предложена методика количественного определения его в мази "Бисопролозоль" методом спектрофотометрии, являющимся альтернативой титриметрическим методам анализа, с погрешностью, не превышающей ±1,89 %. Процедурой валидации доказаны её специфичность, линейность, правильность и прецизионность. Полученные результаты удовлетворяют критериям приемлемости. Разработанная методика спектрофотометрического анализа селективного бета-адреноблокатора в фармакологической композиции "Бисопролозоль" может быть рекомендована для включения в нормативно-техническую документацию в раздел количественного определения компонентов мази, что позволит устанавливать качество её приготовления. Список литературы 1. Государственная фармакопея Российской Федерации. XIV издание. ФС.2.1.0071.18 Бисопролола фумарат. [Электронный ресурс]. Режим доступа: https://femb.ru/record/pharmacopea14. (дата обращения 15.04.2022). 2. Емельянова И.В., Махотина М.В., Емельянов А.А., Емельянов А.А., Хидирова З. А., авторы; Общество с ограниченной ответственностью "Общество лабораторных исследований медицинских препаратов", патентообладатель. Способ получения аквакомплекса глицеросольвата титана – Тизоля. Российская Федерация патент RU 2720459. 30 апреля 2020. 3. Замараева А.И., Бессонова Н.С., Кобелева Т.А., Сичко А.И. Количественный спектрофотометрический анализ лекарственного препарата "Метрокетоконазоль". Вопросы обеспечения качества лекарственных средств 2020; 4(30): 21-27. 4. Кобелева Т.А., Сичко А.И., Попова М.И., Шаповалова Е.М. Разработка и валидация спектрофотометрического способа анализа пропранолола в новой мягкой лекарственной форме "Пропранозоль". Человек и его здоровье 2021; 24(4):83-90. 5. Леоте-Лабрезе К., Дюма де ля Рок Э., Тэеб А., Тамбо Ж.-Б., авторы; Юниверсите Виктор Сегален-Бордо, патентообладатель. Применение бета-блокатора для изготовления лекарственного средства для лечения гемангиом. Российская Федерация патент RU 2471500. 10 января 2013 г. 6. Talmaciu M.M., Bodoki E., Oprean R. Global chemical reactivity parameters for several chiral beta-blockers from the Density Functional Theory viewpoint. Clujul Medical 2016; 89(4): 513-518.
Corresponding Author: Kobeleva Tatyana; e-mail: kobeleva@tyumsmu.ru. Funding. The study had no sponsorship. Conflict of interest. None declared. Abstract Introduction. When developing new pharmacologically active compositions and introducing them into extemporaneous manufacturing and industrial production, a comprehensive study of the properties of the medicinal product applying modern methods of analysis combining high metrological characteristics, expressiveness, sensitivity, accuracy, availability, reliability is mandatory. Development of analytical methods for quality control of new drug compositions is an urgent task of modern pharmaceutical analysis. Aim. Development and validation of a method for quantitative determination of bisoprolol in a new pharmacological composition "Bisoprolozol". Material and methods. To perform the analysis, we used pharmaceutical substance bisoprolol fumarate, glycerol hydrophilic gel "Tizol", ointment "Bisoprolozol" consisting of 0,5% of selective beta-blocker in titanium-containing glycerohydrogel. During the experiment, spectrophotometer SF-2000 and the method of absorption spectrophotometry in the ultraviolet region were used. Regression analysis of data obtained was performed in Microsoft Office Excel 2016 (OFS.1.1.0013.15 "Statistical processing of the results of chemical experiment"). The technique was evaluated according to validation parameters: specificity, linearity, correctness, and precision. Results. Studying the electronic spectral curves of bisoprolol we determined that its analysis is rationally performed at a wavelength of 274 nm (experimentally determined maximum absorption). In the course of the study we determined the sensitivity of the determination of the drug, which is equal to 5.260 µg/ml at A(min) = 0.02. The results of quantitative analysis of bisoprolol in the pharmacological composition "Bisoprolozol" showed that the mass of the selective blocker of adrenergic receptors (0.0409-0.0536 g) is within the acceptable limits according to the regulatory documentation for soft pharmaceutical forms (Order of the Russian Ministry of Health № 751n of 26.10.2015). Conclusion. In the present experiment, optimal conditions for the spectrophotometric method of analysis were selected, based on which the method of quantitative determination of bisoprolol in the new pharmacological composition "Bisoprolozol" with an error not exceeding ± 1.89 % was developed, validated and presented. Key words bisoprolol, gel "Tizol", spectrophotometry, validation, quantitative determination References 1. Gosudarstvennaya farmakopeya Rossiyskoy Federatsii. XIV izdanie FS.2.1.0071.18. Bisoprolola fumarat [State Pharmacopoeia of Russian Federation. 14th edition FS.2.1.0071.18. Bisoprol fumarate]. Available at: https://femb.ru/record/pharmacopea14. Accessed: 15.04.2022. (In Russ.) 2. Emelyanova I.V., Makhotina M.V., Emelyanov A.A., Emelyanov A.A., Khidirova Z.A., inventors; Obshchestvo s ogranichennoj otvetstvennostyu "Obshchestvo laboratornykh issledovanij meditsinskikh preparatov", assignee. Sposob polucheniya akvakompleksa glitserosol'vata titana – Tizolya. [Method of producting aqua-complex of titanium glycerol-solvate – Tizolum]. Russian Federation patent RU 2720459. 2020 April 30. (In Russ.) 3. Zamaraeva A.I., Bessonova N.S., Kobeleva T.A., Sichko A.I. Kolichestvennyi spektrofotometricheskii analiz lekarstvennogo preparata "Metroketokonazol'". [Spectrophotometric analysis of a new drug "Metroketoconazole"]. Voprosy obespecheniya kachestva lekarstvennykh sredstv [Journal of pharmaceuticals quality assurance issue] 2020; 4(30): 21-27. (In Russ.). 4. Kobeleva T.A., Sichko A.I., Popova M.I., Shapovalova E.M. Razrabotka i validatsiya spektrofotometricheskogo sposoba analiza propranolola v novoi myagkoi lekarstvennoi forme "Propranozol'". [Development and validation of a spectrophotometric method for the analysis of propranolol in a new soft dosage form "Propranozol"]. Chelovek i ego zdorov'e [Humans and their health] 2021; 24(4): 83-90. (In Russ.). 5. Leothe-Labrese K., Dumas de la Roque E., Thaeb A., Tambo J.B., inventors; Universite Viktor Segalen-Bordo, assignee. Primenenie beta-blokatora dlya izgotovleniya lekarstvennogo sredstva dlya lecheniya gemangiom. [Use of beta blocker for preparing drug for treating hemangiomas]. Russian Federation patent RU 2471500. 2013 Jan 10 (In Russ.). 6. Talmaciu M.M., Bodoki E., Oprean R. Global chemical reactivity parameters for several chiral beta-blockers from the Density Functional Theory viewpoint. Clujul Medical 2016; 89(4):513-518. |
[ См. также ] Рубрики |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
Журнал «Медицина» © ООО "Инновационные социальные проекты"
|