| О журнале | Редколлегия | Редсовет | Архив номеров | Поиск | Авторам | Рецензентам | English |
Эффекты эноксапарина в лечебных и терапевтических дозах при COVID-19: систематический обзор и мета-анализ
Автор для корреспонденции: Виноградова Анжела Дмитриевна; e-mail: an.vino97@mail.ru. Финансирование. Исследование не имело спонсорской поддержки. Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов. Аннотация Тромботические осложнения являются одними из наиболее опасных проявлений COVID-19, что обосновывает необходимость антикоагулянтной терапии при новой коронавирусной инфекции. Эффекты эноксапарина в лечебных и профилактических дозах при COVID-19 оценивали по результатам мета-анализа 5 рандомизированных клинических исследований (РКИ). Поиск РКИ был осуществлен в базах данных MEDLINE, Cochrane, PubMed и ClinicalTrials.gov. Расчет отношения шансов (OR) с указанием 95% доверительного интервала и гетерогенности был проведен с помощью программы RevMan 5.4.1. Критерием эффективности антикоагулянтной терапии была комбинированная точка, включающая в себя летальность и тромботические события (артериальные и венозные тромбозы). Безопасность эноксапарина оценивали по частоте кровотечений (вторичные исходы). Статистически значимых различий летальности пациентов с COVID-19, получавших эноксапарин в лечебных дозах по сравнению с профилактическими дозами обнаружено не было [ОR = 0,98; 95% ДИ 0,84 – 1,16; p = 0,85]. Частота тромбозов и тромбоэмболий при использовании эноксапарина в лечебных дозах была ниже по сравнению с профилактическими дозами [ОR = 0,80; 95% ДИ 0,66 – 0,98; p = 0,03], тогда как частота кровотечений была выше [ОR = 2,11; 95% ДИ 1,36 – 3,30; p = 0,0009]. Проведенный мета-анализ позволяет предположить большую эффективность эноксапарина в лечебных дозах для уменьшения частоты тромботических осложнений у госпитализированных больных COVID-19, однако эти данные требуют уточнения. Необходимо дальнейшее проведение многоцентровых рандомизированных контролируемых исследований для выяснения оптимальных режимов антикоагулянтной терапии у больных COVID-19. Ключевые слова мета-анализ, систематический обзор, эноксапарин, COVID-19 doi: 10.29234/2308-9113-2022-10-2-41-55 Для цитирования: Виноградова А. Д., Демидова М. А. Эффекты эноксапарина в лечебных и терапевтических дозах при COVID-19: систематический обзор и мета-анализ. Медицина 2022; 10(2): 41-55. Введение Гиперкоагуляция является одним из наиболее распространённых и опасных внелегочных проявлений новой коронавирусной инфекции COVID-19. Развитие артериальных и венозных тромбозов и тромбоэмболий оказывает негативное влияние на течение болезни. Наиболее характерным для COVID-19 тромботическим паттерном (по результатам вскрытий – около 60% случаев) является тромбоэмболия лёгочной артерии (ТЭЛА), способствующая увеличению летальности [1]. Коагулопатия при COVID-19 характеризуется увеличением уровня D-димера, гиперфибриногенемией, тромбоцитопенией, повышенной частотой тромбоэмболий, а также возможностью развития диссеминированного внутрисосудистого свертывания [2-7]. Согласно Временным методическим рекомендациям Минздрава РФ по профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19) [8] назначение низкомолекулярных гепаринов (НМГ) (или других антикоагулянтов – фондапаринукса, нефракционированного гепарина), как минимум в профилактических дозах, показано всем стационарным пациентам. Необходимость назначения НМГ всем госпитализированным больным COVID-19 при отсутствии противопоказаний представлена также в рекомендациях ISTH – международного общества тромбоза и гемостаза [9]. НМГ обладают противовоспалительными свойствами, что может быть дополнительным преимуществом при инфекции COVID, когда заметно повышен уровень провоспалительных цитокинов и возможно развитие "цитокинового шторма" [10]. Настоящее исследование предназначено для сравнительного анализа применения эноксапарина в профилактических и лечебных дозах в отношении первичных (летальность) и вторичных (тромботические и геморрагические осложнения) исходов с целью определения оптимального режима дозирования НМГ при COVID-19. Материалы и методы исследования Исследование выполнено в соответствии с методическими рекомендациями Центра экспертизы и контроля качества медицинской помощи Министерства здравоохранения Российской Федерации (ФГБУ ЦЭККМП Минздрава России) по проведению мета-анализа (2017) [11]. Поиск результатов клинических исследований был осуществлён в международных базах данных MEDLINE, Cochrane, PubMed и ClinicalTrials.gov по следующим ключевым словам: антикоагулянты, COVID-19, нефракционированный гепарин, низкомолекулярный гепарин, эноксапарин. Ограничения по языку отсутствовали, по датам публикаций – 2020-2021 г. Архив клинических исследований (ClinicalTrials.gov) использовали для поиска конкретных РКИ. Для мета-анализа осуществляли отбор клинических исследований, которые соответствовали критериям включения/исключения. Для каждого из включенных в мета-анализ источников проводили оценку методического качества (в баллах) и статистической гетерогенности результатов по значению индекса гетерогенности I2. В мета-анализ включали клинические исследования, в которых имелась информация об эффективности и безопасности эноксапарина у стационарных больных COVID-19. Извлечение данных из публикаций и протоколов исследований было проведено одним специалистом. По каждой публикации анализировали число включенных пациентов с COVID-19, их клинические характеристики, в том числе тяжесть исходного состояния, используемые антикоагулянты и их дозы (лечебные, промежуточные и профилактические), выживаемость или летальность пациентов, тромботические осложнения и их клинические проявления (тромбоз глубоких вен (ТГВ), ТЭЛА, инсульт, инфаркт), геморрагические осложнения. Результаты применения эноксапарина оценивали по комбинированным точкам, включающим первичные (летальность) и вторичные (тромботические и геморрагические осложнения) исходы. Для оценки качества включённых РКИ были использованы методические рекомендации ФГБУ ЦЭККМП Минздрава России по проведению мета-анализа (2017) и по оценке сравнительной клинической эффективности и безопасности лекарственного препарата (2016) [12]. По каждому включенному в исследование РКИ оценивали риск систематических ошибок. Использовали шкалы анализа условий изучения лекарственного препарата (ЛП) и анализа методологического качества клинических исследований. Шкалу анализа условий изучения ЛП использовали для расчёта поправочного коэффициента. Для РКИ хорошего качества поправочный коэффициент был равен максимальному значению – 1. Шкалу анализа методологического качества применяли для оценки качества каждого РКИ в баллах. РКИ высокого качества по данной шкале имели 9 и более баллов, среднего качества – 7-8 баллов, низкого качества 6 и менее. Для выполнения мета-анализа использовали бесплатное сертифицированное программное обеспечение Кокрановского сотрудничества RevMan 5.4.1. Рассчитывали отношение шансов (OR – англ. Odds Ratio) с указанием 95% доверительного интервала, гетерогенность, статистическую значимость результатов. Статистически значимыми считали различия при уровне вероятности 95% и более (p<0,05). По результатам исследования осуществляли построение форест-диаграмм. Результаты исследования и их обсуждение По выбранным ключевым словам было найдено 203 публикации, из них 44 систематических обзора. 40 из 44 найденных систематических обзоров были удалены на этапе просмотра заголовков и резюме, данные 4 систематических обзоров использовали для обсуждения результатов. Из 20 найденных РКИ критериям отбора соответствовали 5 исследований. Эти исследования носили завершенный характер и содержали информацию об эффективности и безопасности эноксапарина у стационарных больных COVID-19: ATTACC [13], ACTION [14], RAPID [15], INSPIRATION [16], HEP-COVID [17]. ATTACC (Antithrombotic Therapy to Ameliorate Complications of COVID-19) – интервенциональное, проспективное, открытое контролируемое, рандомизированное клиническое исследование адаптивного дизайна, предпринятое с целью доказательства эффективности применения низкомолекулярного гепарина эноксапарина в терапевтических дозах (1,5 мг/кг подкожно 1 раз в день или 1 мг/кг 2 раза в день) по сравнению с эффектами тинзапарина (4500 МЕ подкожно), далтепарина (5000 МЕ подкожно) или нефракционированного гепарина (НФГ) (5000 МЕ подкожно 3 раза в день) в профилактических дозах. В исследовании участвовало 1200 (536/567) пациентов в возрасте 18 и старше лет с подтверждённым диагнозом новая коронавирусная инфекция COVID-19 без сопутствующих на момент госпитализации тромбозов и тромбоэмболий. Длительность исследования – 1 год, время наблюдения за пациентами 14 дней, наблюдение летальности – 21 день, наблюдение артериальных и венозных тромбоэмболических событий – 28 и 90 дней. ACTION (Randomized Clinical Trial to Evaluate a Routine Full Anticoagulation Strategy in Patients With Coronavirus (COVID-19)) – интервенциональное, слепое, контролируемое, многоцентровое РКИ, направленное на доказательство эффективности применения эноксапарина в лечебных дозах (1 мг/кг подкожно 2 раза в день) по сравнению с идентичной терапией COVID-19, но с использованием эноксапарина в профилактических дозах (40-60 мг/сутки). В исследовании участвовало 615 (310/304) пациентов 18 лет и старше с подтверждённым диагнозом новая коронавирусная инфекция COVID-19, имевших повышенную концентрацию D-димера в крови. Длительность исследования – 1 год 1 месяц, время наблюдения за пациентами – 30 дней. RAPID (Coagulopathy of COVID-19: A Pragmatic Randomized Controlled Trial of Therapeutic Anticoagulation Versus Standard Care as a Rapid Response to the COVID-19 Pandemic) – интервенциональное, двунаправленное, многоцентровое, открытое контролируемое РКИ, направленное на оценку эффективности эноксапарина в терапевтических дозах (1 мг/кг подкожно два раза в день, 1,5 мг/кг – 1 раз в день) по сравнению с эффектами эноксапарина (40 мг 2 раза в сутки) и других антикоагулянтов – далтепарина (5000 МЕ 1-2 раза в сутки), тинзапарина (4500-9000 МЕ / сутки), фондапаринукса (2,5 мг / сутки), НФГ (5000-7500 МЕ каждые 8-12 ч) в профилактических дозах. В исследовании участвовало 465 (228/237) пациентов 18 лет и старше с подтверждённым диагнозом коронавирусная инфекция COVID-19, имевших повышенную концентрацию D-димера в крови. Длительность исследования – 1 год 5 месяцев, время наблюдения за пациентами – 28 дней. INSPIRATION (Intermediate-dose Versus Standard Prophylactic Anticoagulation In cRitically-ill pATIents With COVID-19: An opeN Label Randomized Controlled Trial – A Randomized Trial of Atorvastatin vs. Placebo In Critically-ill Patients With COVID-19) – интервенциональное, многоцентровое, ослепленное (со слепой оценкой результатов), рандомизированное плацебо контролируемое клиническое исследование, в котором сравнивались эффекты эноксапарина в дозах 50-110 мг и 30-40 мг в день. В исследовании участвовало 600 (296/294) пациентов 18 лет и старше с подтверждённым диагнозом коронавирусная инфекция COVID-19, имевших повышенную концентрацию D-димера в крови. Длительность исследования – 1 год 1 месяц, время наблюдения за пациентами – 30 дней. HEP-COVID (Systemic Anticoagulation With Full Dose Low Molecular Weight Heparin (LMWH) Vs. Prophylactic or Intermediate Dose LMWH in High Risk COVID-19 Patients) – интервенциональное, многоцентровое, тройное слепое, рандомизированное клиническое исследование, направленное на доказательство эффективности применения эноксапарина в терапевтических дозах (1 мг/кг подкожно 2 раза в день) у пациентов с COVID-19 в критическом состоянии по сравнению с профилактическими дозами эноксапарина (30-60 мг/сутки) или промежуточными дозами НФГ (5000-7500 МЕ). В исследовании участвовало 257 (129/124) пациентов 18 лет и старше с подтверждённым диагнозом новая коронавирусная инфекция COVID-19, имевших повышенную концентрацию D-димера в крови, потребность в кислородной поддержке. Длительность исследования – 1 год 5 месяцев, время наблюдения за пациентами – 30 дней. Анализ методологического качества данных РКИ показал, что одно из них было низкого качества, остальные – удовлетворительного и высокого. Результаты оценки методологического качества каждого РКИ приведены в таблице 1. Таблица 1. Оценка методологического качества РКИ, включенных в мета-анализ.
Примечание: поправочный коэффициент = 1 (популяция соответствует заявленному показанию)*1(ЛП включены в анализируемый перечень)*1 (учтён основной исход) = 1; качество исследований: 6 баллов и менее – низкое, 7-8 – удовлетворительное, 9 и более – высокое. При оценке риска систематических ошибок отмечено, что процедура рандомизации была подробно описана в 4 включённых исследованиях, в РКИ INSPIRATION описания процедуры рандомизации отмечено не было. "Ослепление" персонала предполагалось в ACTION, INSPIRATION и HEP-COVID, а пациентов – только в HEP-COVID, что повышает риск возникновения систематической ошибки дизайна. Ни в одном из исследований не указан конфликт интересов, практически не было затруднений в представлении результатов или восполнении пропусков в данных, за исключением РКИ INSPIRATION. Однако у RAPID, INSPIRATION и HEP-COVID были отмечены дополнительные источники возможных систематических ошибок, что несколько снижало качество проводимых исследований. Результаты анализа риска систематических ошибок для каждого включенного в мета-анализ РКИ представлены в таблице 2. Таблица 2. Анализ риска систематических ошибок РКИ, включённых в мета-анализ.
Примечание: + – низкий риск, +/- – неопределённый риск, – – высокий риск. Таким образом, наименьший суммарный риск систематических ошибок был отмечен для РКИ ACTION и HEP-COVID, и, следовательно, их можно считать наиболее качественно проведёнными. Эффективность применения антикоагулянтов оценивали по их влиянию на частоту летального исхода и тромботических событий (артериальные и венозные тромбозы (тромбозы глубоких вен (ТГВ), тромбоэмболии лёгочной артерии (ТЭЛА)), инфаркт миокарда, инсульт), безопасность – по частоте геморрагических проявлений. Мета-анализ показал отсутствие статистических значимых различий в частоте летального исхода у больных COVID-19, получавших эноксапарин в терапевтических и профилактических дозах [ОR = 0,98; 95% ДИ (0,84 – 1,16); p = 0,85] (рис. 1). Как видно из представленной форест-диаграммы статистически значимое снижение частоты летального исхода у пациентов с COVID-19, получавших эноксапарин в терапевтических дозах по сравнению с профилактическими дозами, было отмечено только в одном исследовании HEP-COVID. Следует отметить, что частота тромботических событий при использовании лечебных доз антикоагулянтов по сравнению с профилактическими была меньше [ОR = 0,80; 95% ДИ (0,66 – 0,98); p = 0,03], однако в 4-х из 5 РКИ данные не были статистически значимыми (рис. 2). Рис. 1. Отношение шансов смертельных исходов при использовании эноксапарина в терапевтических и профилактических дозах у пациентов с COVID-19. 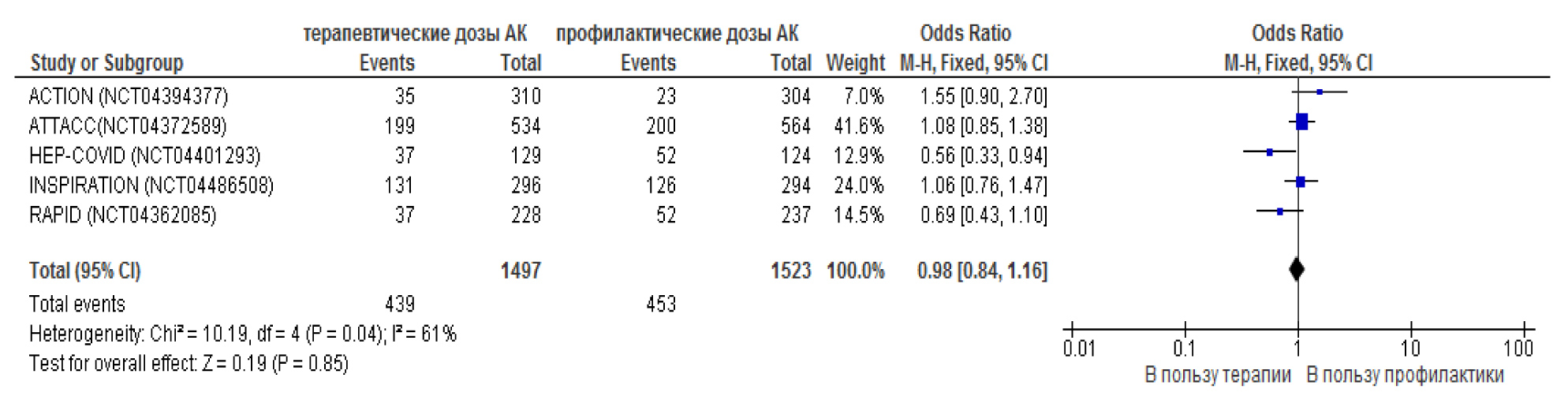 Рис. 2. Отношение шансов тромботических событий при использовании эноксапарина в терапевтических и профилактических дозах у пациентов с COVID-19. 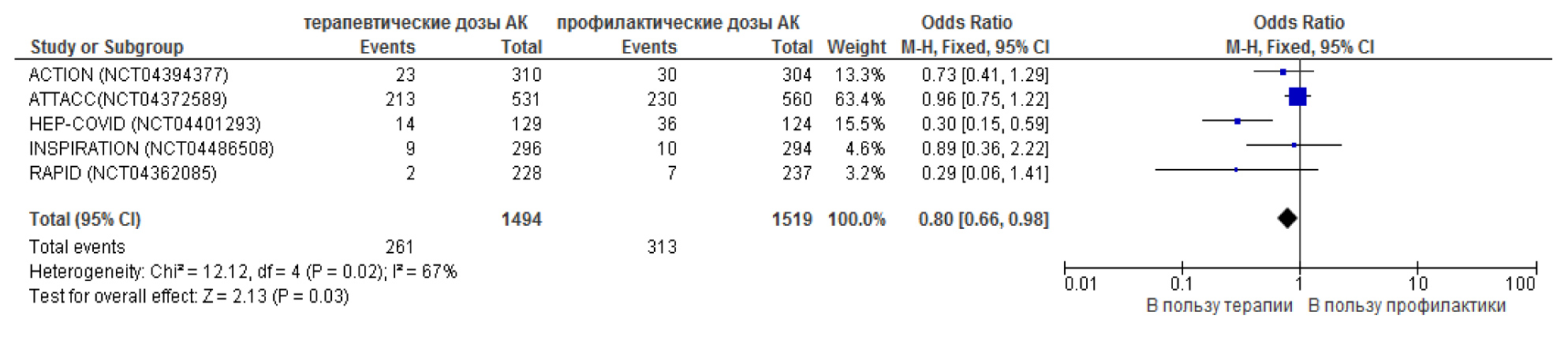 Полученные сведения позволяют предположить снижение частоты тромбозов и тромбоэмболий, а также случаев ТГВ, ТЭЛА, инфаркта миокарда и инсульта у пациентов с новой коронавирусной инфекцией COVID-19 при назначении эноксапарина в лечебных дозах по сравнению с профилактическими. Безопасность антикоагулянтной терапии оценивали по частоте геморрагических событий, включавших большое кровотечение или клинически значимое небольшое кровотечение. Анализ данных РКИ продемонстрировал ожидаемое увеличение числа случаев крупных геморрагий при применении антикоагулянта в лечебных дозах по сравнению с профилактическими [ОR = 2,11; 95% ДИ (1,36 – 3,30); p = 0,0009]. В 4-х из 5 РКИ результаты не были статистически значимыми (рис. 3). Рис. 3. Отношение шансов геморрагических событий при использовании эноксапарина в терапевтических и профилактических дозах у пациентов с COVID-19. 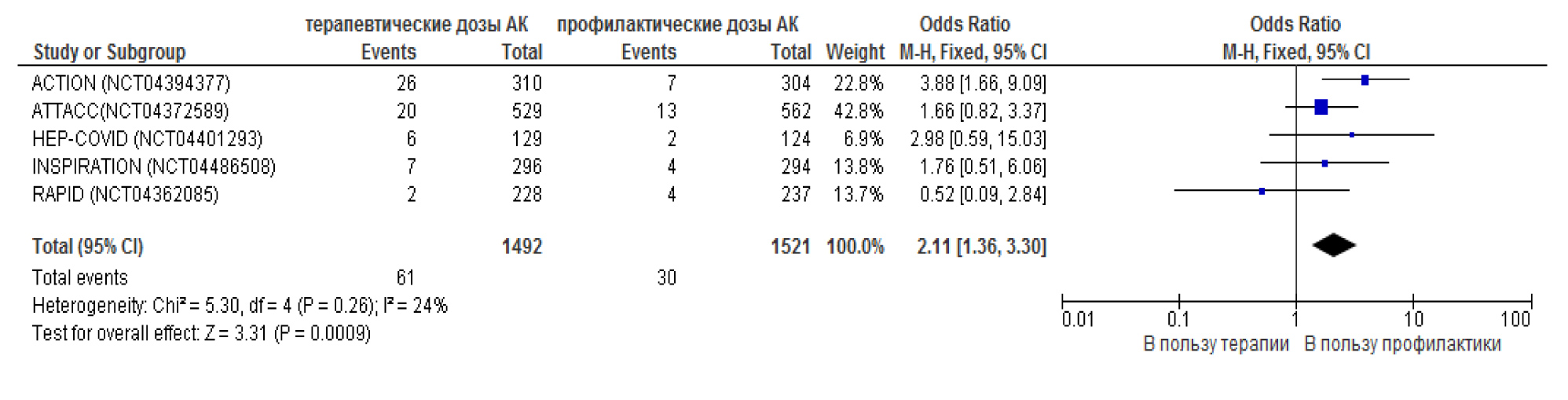 Результаты мета-анализа показали большую безопасность применения НМГ в профилактических дозах по сравнению с лечебными, однако данные требуют уточнения, так как статистически значимые результаты были получены только в исследовании ACTION. В связи с высоким риском систематических ошибок в исследованиях RAPID и INSPIRATION для всех включенных в мета-анализ РКИ проводили анализ чувствительности результатов (табл. 4). Таблица 4. Анализ чувствительности результатов исследования эффективности и безопасности антикоагулянтов при COVID-19.
РКИ ATTACC, ACTION, и HEP-COVID подтвердили большую безопасность применения антикоагулянтов в профилактических дозах и отсутствие статистически значимых различий в летальности и частоте тромботических событий при использовании антикоагулянтов в лечебных и профилактических дозах. Проблема повышения эффективности антикоагулянтной терапии при новой коронавирусной инфекции по-прежнему является актуальной. Дискутабельным остается вопрос о выборе доз антикоагулянтов (профилактические, промежуточные или лечебные) для фармакотерапии коагулопатии, связанной с COVID-19. Исследования для выяснения оптимального режима антикоагулянтной терапии при COVID-19 продолжаются, одним из них является многоцентровое РКИ FREEDOM COVID-19 [18]. В большинстве завершенных РКИ показано снижение риска летального исхода у госпитализированных пациентов с COVID-19 при проведении антикоагулянтной терапии в лечебных дозах по сравнению с ее отсутствием [19-32]. Следует отметить, что в исследовании Al-Samkari H. et al. [33] с включением 2809 больных COVID-19 не было выявлено статистически значимого влияния антикоагулянтной терапии на выживаемость больных с COVID-19. В исследовании Nadkarni G. N. et al. (2020) сообщалось о снижении риска госпитальной летальности от всех причин пациентов с COVID-19 при назначении антикоагулянтов в терапевтических дозах (ОR= 0,86; 95% ДИ: 0,73–1,02) [26]. В частности, у пациентов отделения интенсивной терапии (ОИТ) применение антикоагулянтов в лечебных дозах было связано со сниженным риском летальных исходов (ОR = 0,30; 95% ДИ: 0,15–0,60; I2: 58%) по сравнению с терапией в профилактических дозах. Однако первое также было связано с более высоким риском кровотечения (ОR = 2,53; 95% ДИ: 1,60–4,00; I2: 65%). Использование антикоагулянтов, главным образом гепарина, снизило смертность от всех причин у пациентов с COVID-19 во время госпитализации [34]. В других исследованиях [25,26,32] отмечено снижение госпитальной летальности при использовании антикоагулянтов как в лечебной, так и профилактической дозе, по сравнению отсутствием антикоагулянтной терапии. В исследовании Ferguson J. et al. (2020) показано отсутствие статистически значимых различий в 28-дневной летальности пациентов, получавших антикоагулянты в лечебной или профилактической дозах (ОR = 0,73; 95 % ДИ: 0,33–1,76) [34,35]. Наибольший эффект от применения антикоагулянтной терапии отмечался у пациентов ОИТ с более высоким риском коагулопатии, вызванной сепсисом, или с заметно повышенным уровнем D-димера [36]. В связи с тем, что частота геморрагических осложнений при применении высоких доз антикоагулянтов выше, чем при использовании профилактических [37] было высказано мнение [38], что антикоагулянтную терапию в терапевтических дозах следует использовать на самых ранних этапах заболевания, когда риск тромбоза высок. В дальнейшем, если нет иных показаний, то дозу следует постепенно снижать до профилактической. Заключение Проведенный мета-анализ позволяет предположить большую эффективность эноксапарина в лечебных дозах по сравнению с профилактическими для уменьшения частоты тромботических осложнений у госпитализированных больных COVID-19, однако эти данные требуют уточнения. Необходимо дальнейшее проведение многоцентровых рандомизированных контролируемых исследований для выяснения оптимальных режимов антикоагулянтной терапии у больных COVID-19. Список литературы 1. Manolis A.S., Manolis T.A., Manolis A.A. et al. COVID-19 Infection: Viral Macro- and Micro-Vascular Coagulopathy and Thromboembolism/Prophylactic and Therapeutic Management. Journal of cardiovascular pharmacology and therapeutics 2021; 26(1): 12-24, doi: 10.1177/1074248420958973 2. Chen E.C., Zon R.L., Battinelli E.M., Connors J.M. Approach to the Patient with COVID-19-Associated Thrombosis: A Case-Based Review. The Oncologist 2020; 25(10): е1500-е1508, doi: 10.1634/theoncologist.2020-0682 3. Colling M.E., Kanthi Y. COVID-19-associated coagulopathy: An exploration of mechanisms. Vascular Medicine 2020; 25(5): 471-478, doi: 10.1177/1358863X20932640 4. Franchini M., Marano G., Cruciani M. et al. COVID-19-associated coagulopathy. Diagnosis 2020; 7(4): 357-363, doi: 10.1515/dx-2020-0078 5. Giannis D., Ziogas I.A., Gianni P. Coagulation disorders in coronavirus infected patients: COVID-19, SARS-CoV-1, MERS-CoV and lessons from the past. Journal of Clinical Virology 2020; 127: 104362. doi: 10.1016/j.jcv.2020.104362 6. Iba T., Connors J.M., Levy J.H. The coagulopathy, endotheliopathy, and vasculitis of COVID-19. Inflammation Research 2020; 69(12): 1181-1189, doi:10.1007/s00011-020-01401-6 7. Katneni U.K., Alexaki A., Hunt R.C. et al. Coagulopathy and Thrombosis as a Result of Severe COVID-19 Infection: A Microvascular Focus. Thrombosis and Haemostasis 2020; 120(12): 1668-1679, doi:10.1055/s-0040-1715841 8. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 15. 2022. [Электронный ресурс]. Режим доступа: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/059/392/original/ВМР_COVID-19_V15.pdf (дата обращения: 12.03.2022). 9. Thachil J., Tang N., Gando S. et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. Journal of thrombosis and haemostasis 2020; 18(5): 1023-1026, doi: 10.1111/jth.14810 10. Poterucha T.J., Libby P., Goldhaber S.Z. More than an anticoagulant: do heparins have direct anti-inflammatory effects? Thrombosis and Haemostasis 2017; 117(3): 437-444, doi: 10.1160/TH16-08-0620 11. Методические рекомендации по проведению мета-анализа. 2017. [Электронный ресурс]. Режим доступа: https://rosmedex.ru/wp-content/uploads/2018/01/Metodicheskie-rekomendatsii-po-provedeniyu-meta-analiza-2017-g..pdf (дата обращения: 12.12.2021). 12. Методические рекомендации по оценке сравнительной клинической эффективности и безопасности лекарственного препарата. 2016. [Электронный ресурс]. Режим доступа: https://rosmedex.ru/wp-content/uploads/2016/12/MR-E%60B-23.12.2016.pdf (дата обращения: 12.12.2021). 13. Goligher E.C, Bradbury C.A, McVerry B.J. et al. Therapeutic Anticoagulation with Heparin in Critically Ill Patients with Covid-19. The New England journal of medicine 2021; 385(9): 777-789, doi: 10.1056/NEJMoa2103417 14. Lopes R.D., de Barros E. Silva P.G.M., Furtado R.H.M. et al. Therapeutic versus prophylactic anticoagulation for patients admitted to hospital with COVID-19 and elevated D-dimer concentration (ACTION): an open-label, multicentre, randomised, controlled trial. Lancet 2021; 397(10291): 2253-2263, doi: 10.1016/S0140-6736(21)01203-4 15. Sholzberg M., Tang G.H., Rahhal H. et al. Effectiveness of therapeutic heparin versus prophylactic heparin on death, mechanical ventilation, or intensive care unit admission in moderately ill patients with COVID-19 admitted to hospital: RAPID randomised clinical trial. British medical journal 2021; 375(2400), doi: 10.1136/bmj.n2400 16. Sadeghipour P., Talasaz A.H., Rashidi F. et al. Effect of Intermediate-Dose vs Standard-Dose Prophylactic Anticoagulation on Thrombotic Events, Extracorporeal Membrane Oxygenation Treatment, or Mortality Among Patients With COVID-19 Admitted to the Intensive Care Unit: The INSPIRATION Randomized Clinical Trial. Journal of the American Medical Association 2021; 325(16): 1620-1630, doi: 10.1001/jama.2021.4152 17. Spyropoulos A.C., Goldin M., Giannis D. et al. Efficacy and Safety of Therapeutic-Dose Heparin vs Standard Prophylactic or Intermediate-Dose Heparins for Thromboprophylaxis in High-risk Hospitalized Patients With COVID-19: The HEP-COVID Randomized Clinical Trial. Journal of the American Medical Association 2021; 181(12): 1612-1620, doi: 10.1001/jamainternmed.2021.6203 18. Farkouh M. E., Stone G. W., Lala A. et al. Anticoagulation Strategy [FREEDOM COVID]. (2022). Anticoagulation in Patients With COVID-19: JACC Review Topic of the Week. Journal of the American College of Cardiology 2022; 79(9): 917-928 19. Ayerbe L., Risco C., Ayis S. The association between treatment with heparin and survival in patients with Covid-19. Journal of thrombosis and thrombolysis 2020; 50(2): 298-301, doi: 10.1007/s11239-020-02162-z 20. Paranjpe I., Fuster V., Lala A. et al. Association of Treatment Dose Anticoagulation with In-Hospital Survival Among Hospitalized Patients With COVID-19. Journal of the American College of Cardiology 2020; 76(1): 122-124, doi: 10.1016/j.jacc.2020.05.001 21. Desai A., Voza G., Paiardi S. et al. The role of anti-hypertensive treatment, comorbidities and early introduction of LMWH in the setting of COVID-19: A retrospective, observational study in Northern Italy. International journal of cardiology 2021; 324: 249-254, doi: 10.1016/j.ijcard.2020.09.062 22. Hsu A., Liu Y., Zayac A.S. et al. Intensity of anticoagulation and survival in patients hospitalized with COVID-19 pneumonia. Thrombosis research 2020; 196: 375-378, doi: 10.1016/j.thromres.2020.09.030 23. Gonzalez-Porras J.R., Belhassen-Garcia M., Lopez-Bernus A. et al. Low molecular weight heparin is useful in adult COVID-19 inpatients. Experience during the first Spanish wave: observational study. São Paulo medical journal = Revista paulista de medicina 2021; 13: 1516, doi: 10.1590/1516-3180.2021.0098.R1.08062021 24. Albani F., Sepe L., Fusina F. et al. Thromboprophylaxis with enoxaparin is associated with a lower death rate in patients hospitalized with SARS-CoV-2 infection. A cohort study. EClinicalMedicine 2020; 27: 100562, doi: 10.1016/j.eclinm.2020.100562 25. Ionescu F., Jaiyesimi I., Petrescu I. et al. Association of anticoagulation dose and survival in hospitalized COVID-19 patients: A retrospective propensity score-weighted analysis. European journal of haematology 2021; 106(2): 165-174, doi: 10.1111/ejh.13533 26. Nadkarni G.N., Lala A., Bagiella E. et al. Anticoagulation, Bleeding, Mortality, and Pathology in Hospitalized Patients With COVID-19. Journal of the American College of Cardiology 2020; 76(16): 1815-1826, doi: 10.1016/j.jacc.2020.08.041 27. Billett H.H., Reyes-Gil M., Szymanski J. et al. Anticoagulation in COVID-19: Effect of Enoxaparin, Heparin, and Apixaban on Mortality. Thrombosis and haemostasis 2020; 120(12): 1691-1699, doi: 10.1055/s-0040-1720978 28. Falcone M., Tiseo G., Barbieri G. et al. Role of Low-Molecular-Weight Heparin in Hospitalized Patients with Severe Acute Respiratory Syndrome Coronavirus 2 Pneumonia: A Prospective Observational Study. Open forum infectious diseases 2020; 7(12): 563, doi: 10.1093/ofid/ofaa563 29. Qin W., Dong F., Zhang Z. et al. Low molecular weight heparin and 28-day mortality among patients with coronavirus disease 2019: A cohort study in the early epidemic era. Thrombosis research 2021; 198: 19-22, doi: 10.1016/j.thromres.2020.11.020 30. Rentsch C.T., Beckman J.A., Tomlinson L. et al. Early initiation of prophylactic anticoagulation for prevention of COVID-19 mortality: a nationwide cohort study of hospitalized patients in the United States. MedRxiv: the preprint server for health sciences 2020; 20246579, doi: 10.1101/2020.12.09.20246579 31. Shen L., Qiu L., Liu D. et al. The Association of Low Molecular Weight Heparin Use and In-hospital Mortality Among Patients Hospitalized with COVID-19. Cardiovascular drugs and therapy / sponsored by the International Society of Cardiovascular Pharmacotherapy 2021; 1-8, doi: 10.1007/s10557-020-07133-3 32. Di Castelnuovo A., Costanzo S., Antinori A. et al. Heparin in COVID-19 Patients Is Associated with Reduced In-Hospital Mortality: The Multicenter Italian CORIST Study. Thrombosis and haemostasis 2021; 121(8): 1054-1065, doi: 10.1055/a-1347-6070 33. Al-Samkari H., Gupta S., Karp Leaf R. et al. Thrombosis, bleeding, and the effect of anticoagulation on survival in critically ill patients with COVID-19 in the United States. Research and practice in thrombosis and haemostasis 2020; 4 (Suppl 1). Available at: https://abstracts.isth.org/abstract/thrombosis-bleeding-and-the-effect-of-anticoagulation-on-survival-in-critically-ill-patients-with-covid-19-in-the-united-states/ 34. Parisi R., Costanzo S., Di Castelnuovo A. et al. Different Anticoagulant Regimens, Mortality, and Bleeding in Hospitalized Patients with COVID-19: A Systematic Review and an Updated Meta-Analysis. Seminars in thrombosis and hemostasis 2021; 47(4): 372-391, doi: 10.1055/s-0041-1726034 35. Ferguson J., Volk S., Vondracek T. et al. Empiric Therapeutic Anticoagulation and Mortality in Critically Ill Patients With Respiratory Failure From SARS-CoV-2: A Retrospective Cohort Study. Journal of clinical pharmacology 2020; 60(11): 1411-1415, doi: 10.1002/jcph.1749 36. Tang N., Bai H., Chen X. et al. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. Journal of thrombosis and haemostasis 2021; 18(5): 1094-1099, doi: 10.1111/jth.14817 37. Moonla C., Sosothikul D., Chiasakul T. et al. Anticoagulation and In-Hospital Mortality from Coronavirus Disease 2019: A Systematic Review and Meta-Analysis. Clinical and applied thrombosis/hemostasis: official journal of the International Academy of Clinical and Applied Thrombosis/Hemostasis 2021; 27: 10760296211008999, doi: 10.1177/10760296211008999 38. Tacquard C., Mansour A., Godon A. et al. Anticoagulation in COVID-19: not strong for too long? Anaesthesia, critical care and pain medicine 2021; 40(2): 100857, doi: 10.1016/j.accpm.2021.100857
Corresponding Author: Vinogradova Angela; e-mail: an.vino97@mail.ru. Conflict of interest. None declared. Funding. The study had no sponsorship. Abstract Thrombotic complications are the most dangerous manifestations of COVID-19. This justifies the need for anticoagulant therapy in a new coronavirus infection. The effects of enoxaparin at therapeutic and prophylactic doses in COVID-19 were assessed from a meta-analysis of 5 randomized clinical trials (RCTs). Search for RCTs was performed in the MEDLINE, Cochrane, PubMed, and ClinicalTrials.gov databases. Odds ratio (OR) with 95% confidence interval and heterogeneity were calculated applying RevMan 5.4.1 software. Combined criterion for the effectiveness of anticoagulant therapy included mortality and thrombotic events (arterial and venous thrombosis). The safety of enoxaparin was assessed by the frequency of bleeding (secondary outcomes). There were no statistically significant differences in mortality in COVID-19 patients receiving enoxaparin at therapeutic doses compared with prophylactic doses [OR = 0.98; 95% CI 0.84 – 1.16; p = 0.85]. The frequency of thrombosis and thromboembolism when using enoxaparin in therapeutic doses was lower compared with prophylactic doses [OR = 0.80; 95% CI 0.66 – 0.98; p = 0.03], while the frequency of bleeding was higher [OR = 2.11; 95% CI 1.36 – 3.30; p = 0.0009]. This meta-analysis suggests a greater efficacy of enoxaparin at therapeutic doses in reducing the incidence of thrombotic complications in hospitalized COVID-19 patients, however, these data require clarification. Further multicenter randomized controlled trials are needed to determine the optimal anticoagulant regimens in COVID-19 patients. Key words enoxaparin, meta-analysis, systematic review, COVID-19 References 1. Manolis A.S., Manolis T.A., Manolis A.A. et al. COVID-19 Infection: Viral Macro- and Micro-Vascular Coagulopathy and Thromboembolism/Prophylactic and Therapeutic Management. Journal of cardiovascular pharmacology and therapeutics 2021; 26(1): 12-24, doi: 10.1177/1074248420958973 2. Chen E.C., Zon R.L., Battinelli E.M., Connors J.M. Approach to the Patient with COVID-19-Associated Thrombosis: A Case-Based Review. The Oncologist 2020, doi: 10.1634/theoncologist.2020-0682 3. Colling M.E., Kanthi Y. COVID-19-associated coagulopathy: An exploration of mechanisms. Vascular Medicine 2020; 25(5): 471-478, doi: 10.1177/1358863X20932640 4. Franchini M., Marano G., Cruciani M. et al. COVID-19-associated coagulopathy. Diagnosis 2020; 7(4): 357-363, doi: 10.1515/dx-2020-0078 5. Giannis D., Ziogas I.A., Gianni P. Coagulation disorders in coronavirus infected patients: COVID-19, SARS-CoV-1, MERS-CoV and lessons from the past. Journal of Clinical Virology 2020; 127: 104362, doi: 10.1016/j.jcv.2020.104362 6. Iba T., Connors J.M., Levy J.H. The coagulopathy, endotheliopathy, and vasculitis of COVID-19. Inflammation Research 2020; 69(12): 1181-1189, doi: 10.1007/s00011-020-01401-6 7. Katneni U.K., Alexaki A., Hunt R.C. et al. Coagulopathy and Thrombosis as a Result of Severe COVID-19 Infection: A Microvascular Focus. Thrombosis and Haemostasis 2020; 120(12): 1668-1679, doi: 10.1055/s-0040-1715841 8. Vremennye metodicheskie rekomendacii. Profilaktika, diagnostika i lechenie novoj koronavirusnoj infekcii (COVID-19). Versiya 15. [Temporary methodological recommendations. Prevention, diagnosis and treatment of new coronavirus infection (COVID-19). Version 15.] 2022. Available at: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/059/392/original/ВМР_COVID-19_V15.pdf Accessed: 12.03.2022. (In Russ.) 9. Thachil J., Tang N., Gando S. et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. Journal of thrombosis and haemostasis 2020; 18(5): 1023-1026, doi: 10.1111/jth.14810 10. Poterucha T.J., Libby P., Goldhaber S.Z. More than an anticoagulant: do heparins have direct anti-inflammatory effects? Thrombosis and Haemostasis 2017; 117(3): 437-444, doi: 10.1160/TH16-08-0620 11. Metodicheskie rekomendacii po provedeniyu meta-analiza. [Methodological recommendations for conducting meta-analysis.] 2017. Available at: https://rosmedex.ru/wp-content/uploads/2018/01/Metodicheskie-rekomendatsii-po-provedeniyu-meta-analiza-2017-g..pdf Accessed: 12.12.2021. (In Russ.) 12. Metodicheskie rekomendacii po ocenke sravnitel'noj klinicheskoj effektivnosti i bezopasnosti lekarstvennogo preparata. [Methodological recommendations for the evaluation of the comparative clinical efficacy and safety of the drug.] 2016. Available at: https://rosmedex.ru/wp-content/uploads/2016/12/MR-E%60B-23.12.2016.pdf Accessed: 12.12.2021. (In Russ.) 13. Goligher E.C, Bradbury C.A, McVerry B.J. et al. Therapeutic Anticoagulation with Heparin in Critically Ill Patients with Covid-19. The New England journal of medicine 2021; 385(9): 777-789, doi: 10.1056/NEJMoa2103417 14. Lopes R.D., de Barros E. Silva P.G.M., Furtado R.H.M. et al. Therapeutic versus prophylactic anticoagulation for patients admitted to hospital with COVID-19 and elevated D-dimer concentration (ACTION): an open-label, multicentre, randomised, controlled trial. Lancet 2021; 397(10291): 2253-2263, doi: 10.1016/S0140-6736(21)01203-4 15. Sholzberg M., Tang G.H., Rahhal H. et al. Effectiveness of therapeutic heparin versus prophylactic heparin on death, mechanical ventilation, or intensive care unit admission in moderately ill patients with COVID-19 admitted to hospital: RAPID randomised clinical trial. British medical journal 2021; 375(2400), doi: 10.1136/bmj.n2400 16. Sadeghipour P., Talasaz A.H., Rashidi F. et al. Effect of Intermediate-Dose vs Standard-Dose Prophylactic Anticoagulation on Thrombotic Events, Extracorporeal Membrane Oxygenation Treatment, or Mortality Among Patients With COVID-19 Admitted to the Intensive Care Unit: The INSPIRATION Randomized Clinical Trial. Journal of the American Medical Association 2021; 325(16): 1620-1630, doi: 10.1001/jama.2021.4152 17. Spyropoulos A.C., Goldin M., Giannis D. et al. Efficacy and Safety of Therapeutic-Dose Heparin vs Standard Prophylactic or Intermediate-Dose Heparins for Thromboprophylaxis in High-risk Hospitalized Patients With COVID-19: The HEP-COVID Randomized Clinical Trial. Journal of the American Medical Association 2021; 181(12): 1612-1620, doi: 10.1001/jamainternmed.2021.6203 18. Farkouh M. E., Stone G. W., Lala A. et al. Anticoagulation Strategy [FREEDOM COVID]. (2022). Anticoagulation in Patients With COVID-19: JACC Review Topic of the Week. Journal of the American College of Cardiology 2022; 79(9): 917-928 19. Ayerbe L., Risco C., Ayis S. The association between treatment with heparin and survival in patients with COVID-19. Journal of thrombosis and thrombolysis 2020; 50(2): 298-301, doi: 10.1007/s11239-020-02162-z 20. Paranjpe I., Fuster V., Lala A. et al. Association of Treatment Dose Anticoagulation with In-Hospital Survival Among Hospitalized Patients With COVID-19. Journal of the American College of Cardiology 2020; 76(1): 122-124, doi: 10.1016/j.jacc.2020.05.001 21. Desai A., Voza G., Paiardi S. et al. The role of anti-hypertensive treatment, comorbidities and early introduction of LMWH in the setting of COVID-19: A retrospective, observational study in Northern Italy. International journal of cardiology 2021; 324: 249-254, doi: 10.1016/j.ijcard.2020.09.062 22. Hsu A., Liu Y., Zayac A.S. et al. Intensity of anticoagulation and survival in patients hospitalized with COVID-19 pneumonia. Thrombosis research 2020; 196: 375-378, doi: 10.1016/j.thromres.2020.09.030 23. Gonzalez-Porras J.R., Belhassen-Garcia M., Lopez-Bernus A. et al. Low molecular weight heparin is useful in adult COVID-19 inpatients. Experience during the first Spanish wave: observational study. São Paulo medical journal = Revista paulista de medicina 2021; 13: 1516, doi: 10.1590/1516-3180.2021.0098.R1.08062021 24. Albani F., Sepe L., Fusina F. et al. Thromboprophylaxis with enoxaparin is associated with a lower death rate in patients hospitalized with SARS-CoV-2 infection. A cohort study. EClinicalMedicine 2020; 27: 100562, doi: 10.1016/j.eclinm.2020.100562 25. Ionescu F., Jaiyesimi I., Petrescu I. et al. Association of anticoagulation dose and survival in hospitalized COVID-19 patients: A retrospective propensity score-weighted analysis. European journal of haematology 2021; 106(2): 165-174, doi: 10.1111/ejh.13533 26. Nadkarni G.N., Lala A., Bagiella E. et al. Anticoagulation, Bleeding, Mortality, and Pathology in Hospitalized Patients With COVID-19. Journal of the American College of Cardiology 2020; 76(16): 1815-1826, doi: 10.1016/j.jacc.2020.08.041 27. Billett H.H., Reyes-Gil M., Szymanski J. et al. Anticoagulation in COVID-19: Effect of Enoxaparin, Heparin, and Apixaban on Mortality. Thrombosis and haemostasis 2020; 120(12): 1691-1699, doi: 10.1055/s-0040-1720978 28. Falcone M., Tiseo G., Barbieri G. et al. Role of Low-Molecular-Weight Heparin in Hospitalized Patients With Severe Acute Respiratory Syndrome Coronavirus 2 Pneumonia: A Prospective Observational Study. Open forum infectious diseases 2020; 7(12): 563, doi: 10.1093/ofid/ofaa563 29. Qin W., Dong F., Zhang Z. et al. Low molecular weight heparin and 28-day mortality among patients with coronavirus disease 2019: A cohort study in the early epidemic era. Thrombosis research 2021; 198: 19-22, doi: 10.1016/j.thromres.2020.11.020 30. Rentsch C.T., Beckman J.A., Tomlinson L. et al. Early initiation of prophylactic anticoagulation for prevention of COVID-19 mortality: a nationwide cohort study of hospitalized patients in the United States. MedRxiv: the preprint server for health sciences 2020; 20246579, doi: 10.1101/2020.12.09.20246579 31. Shen L., Qiu L., Liu D. et al. The Association of Low Molecular Weight Heparin Use and In-hospital Mortality Among Patients Hospitalized with COVID-19. Cardiovascular drugs and therapy / sponsored by the International Society of Cardiovascular Pharmacotherapy 2021; 1-8, doi: 10.1007/s10557-020-07133-3 32. Di Castelnuovo A., Costanzo S., Antinori A. et al. Heparin in COVID-19 Patients Is Associated with Reduced In-Hospital Mortality: The Multicenter Italian CORIST Study. Thrombosis and haemostasis 2021; 121(8): 1054-1065, doi: 10.1055/a-1347-6070 33. Al-Samkari H., Gupta S., Karp Leaf R. et al. Thrombosis, bleeding, and the effect of anticoagulation on survival in critically ill patients with COVID-19 in the United States. Research and practice in thrombosis and haemostasis 2020; 4. (Suppl 1). Available at: https://abstracts.isth.org/abstract/thrombosis-bleeding-and-the-effect-of-anticoagulation-on-survival-in-critically-ill-patients-with-covid-19-in-the-united-states/ 34. Parisi R., Costanzo S., Di Castelnuovo A. et al. Different Anticoagulant Regimens, Mortality, and Bleeding in Hospitalized Patients with COVID-19: A Systematic Review and an Updated Meta-Analysis. Seminars in thrombosis and hemostasis 2021; 47(4): 372-391, doi: 10.1055/s-0041-1726034 35. Ferguson J., Volk S., Vondracek T. et al. Empiric Therapeutic Anticoagulation and Mortality in Critically Ill Patients With Respiratory Failure From SARS-CoV-2: A Retrospective Cohort Study. Journal of clinical pharmacology 2020; 60(11): 1411-1415, doi: 10.1002/jcph.1749 36. Tang N., Bai H., Chen X. et al. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. Journal of thrombosis and haemostasis 2021; 18(5): 1094-1099, doi: 10.1111/jth.14817 37. Moonla C., Sosothikul D., Chiasakul T. et al. Anticoagulation and In-Hospital Mortality From Coronavirus Disease 2019: A Systematic Review and Meta-Analysis. Clinical and applied thrombosis/hemostasis: official journal of the International Academy of Clinical and Applied Thrombosis/Hemostasis 2021; 27: 10760296211008999, doi: 10.1177/10760296211008999 38. Tacquard C., Mansour A., Godon A. et al. Anticoagulation in COVID-19: not strong for too long? Anaesthesia, critical care and pain medicine 2021; 40(2): 100857, doi: 10.1016/j.accpm.2021.100857 |
[ См. также ] Рубрики |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
Журнал «Медицина» © ООО "Инновационные социальные проекты"
|