Авторы
Копылова А. И.
к.фарм.н., ассистент, кафедра химии и фармакогнозии1
Кобелева Т. А.
д.фарм.н., профессор, заведующий, кафедра химии и фармакогнозии1
Сичко А. И.
д.фарм.н., профессор, профессор, кафедра химии и фармакогнозии1
1ФГБОУ ВО «Тюменский государственный медицинский университет» Минздрава России, г. Тюмень, Российская Федерация
Автор для корреспонденции
Копылова Анна Игоревна; e-mail: KopylovaAI@tyumsmu.ru
Финансирование
Исследование не имело спонсорской поддержки.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Аннотация
Введение. Для внедрения в медицинскую практику новых лекарственных препаратов обязательным этапом является контроль качества, который включает определение количественного содержания действующих компонентов с использованием современных методов фармацевтического анализа. Тизоль гель, входящий в состав мягких лекарственных форм, является самостоятельным фармакологически активным средством, поэтому актуально проводить оценку его содержания в комплексных лекарственных препаратах. Цель. Разработать способ количественного определения тизоля геля и метронидазола в новой мягкой лекарственной форме «Метронидазоль» с применением метода многоволновой спектрофотометрии. Материалы и методы исследования. Для проведения анализа использовали фармацевтическую субстанцию метронидазола, тизоль гель, мазь «Метронидазоль», содержащую 5% нитроимидазола в тизольной основе. Исследования выполняли на спектрофотометре СФ-2000 методом многоволновой спектрофотометрии в УФ-области. На основании опытных данных рассчитывали метрологические параметры разработанной аналитической методики. Результаты и их обсуждение. Экспериментальные исследования позволили обосновать использование ацетатного буферного раствора с рН = 4 в качестве оптимального растворителя для проведения спектрофотометрического анализа тизоля геля и метронидазола в смеси. Согласно полученным УФ-спектрам лекарственных средств были выбраны аналитические длины волн (238 нм – для тизоля геля, 316 нм – для метронидазола). По результатам количественного определения компонентов мази «Метронидазоль» содержание лекарственных средств находится в пределах: метронидазола от 0,4900 до 0,5219 г, тизоля геля (в пересчете на массовую долю титана) – 2,32–2,46%, которые допустимы согласно нормативной документации (ФСП 42-3157-06, ОФС.1.8.0001). Заключение. Впервые предложено проводить количественный анализ тизоля геля в комплексных лекарственных препаратах. Разработан способ количественного определения методом многоволновой спектрофотометрии, позволяющий устанавливать содержание тизоля геля и метронидазола в новой мягкой лекарственной форме «Метронидазоль» с относительными погрешностями среднего результата, не превышающими ± 3,00%.
Ключевые слова
метронидазол, тизоль гель, многоволновая спектрофотометрия, количественное определение
Для цитирования
Копылова А. И., Кобелева Т. А., Сичко А. И. Использование метода многоволновой спектрофотометрии при контроле качества тизоля геля и метронидазола в новой мягкой лекарственной форме «Метронидазоль». Медицина 2024; 12(3): 45-54
DOI
Введение
Метронидазол – химиотерапевтическое средство, обладающее выраженными противомикробным и противопротозойным эффектами. В настоящее время препараты метронидазола находят широкое применение при наружном и местном лечении гинекологических, офтальмологических и стоматологических заболеваний, вызванных патогенными микроорганизмами [7]. Для повышения эффективности антибактериальной терапии предложена новая мягкая лекарственная форма метронидазола и тизоля геля [3].
Ключевым показателем контроля качества нового лекарственного препарата «Метронидазоль» является количественное определение компонентов, обеспечивающих фармакотерапевтический эффект. Тизоль гель применяется как трансдермальный проводник лекарственных средств, обеспечивающий их высокую локальную концентрацию и длительное терапевтическое действие. Титансодержащий гель обладает собственными фармакотерапевтическими эффектами (протекторный, дегидратирующий, анальгезирующий, антифлогистический, антисептический), что доказывает необходимость проведения количественного анализа тизоля в составе новой мази [2,4,6].
Следовательно, целесообразно разрабатывать современный, несложный в проведении, обладающий необходимой точностью и воспроизводимостью способ количественного анализа тизоля геля и метронидазола в новой мягкой лекарственной форме.
Цель исследования
Целью данной работы является разработка способа количественного определения тизоля геля и метронидазола в новой мягкой лекарственной форме «Метронидазоль» с применением метода многоволновой спектрофотометрии.
Материалы и методы исследования
Для проведения анализа использовали фармацевтическую субстанцию метронидазола («Хубэй Хунюань Фармасьютикал Текнолоджи Ко., Лтд.», Китай, ФС.2.1.0136), тизоль гель (ООО «Олимп», Россия, ФСП 42-3157-06), 0,1 моль/л раствор хлористоводородной кислоты (АО «НПИП ”Уралхиминвест”», Россия, ТУ 2642-001-33813273-97), ацетатные буферные растворы с рН 2, 3, 4, 5 (ОФС.1.3.0003), мазь «Метронидазоль», состоящую из 0,5 г метронидазола и 9,5 г тизоля геля. В ходе опытов применяли спектрофотометр марки СФ 2000 (ЗАО «ОКБ СПЕКТР», Россия). Определение количественного содержания метронидазола и тизоля геля проводили методом многоволновой спектрофотометрии в ультрафиолетовой области. Метрологические параметры (относительные погрешности среднего результата (e , %), относительные стандартные отклонения (RSD, %)) рассчитывали на основании опытных данных в соответствии с ОФС.1.1.0013 «Статистическая обработка результатов физических, физико-химических и химических испытаний» [1].
Для применения метода многоволновой спектрофотометрии составили систему уравнений [3], в которой обозначили концентрации действующих компонентов и их молярные коэффициенты экстинкции (для тизоля геля: C1, моль/л, ε1(238), ε1(316); для метронидазола: С2, моль/л, ε2(238), ε2(316)):
А(238) = ε1(238) · С1 + ε2(238) · С2
А(316) = ε1(316) · С1 + ε2(316) · С2
При решении системы представленных уравнений концентрации тизоля геля и метронидазола рассчитывали по формулам (1, 2):
С1=(ε2(316) · А(238) – ε2(238) · А(316))/(ε1(238) · ε2(316) – ε1(316) ·ε2(238)) (1)
С2=(ε1(238) · А(316) – ε1(316) · А(238))/(ε1(238) · ε2(316) – ε1(316) ·ε2(238)) (2)
В ходе количественного анализа метронидазола и тизоля геля в модельной смеси (0,5000 г метронидазола и 9,5000 г тизоля геля) точную массу указанной смеси (около 0,1 г) помещали в мерную колбу и растворяли в 50,0 мл 0,1 моль/л хлористоводородной кислоты. Затем 1,5 мл раствора переносили в мерную колбу емкостью 10,0 мл и ацетатным буферным раствором (рН = 4) доводили объем до метки. Для полученного раствора измеряли оптическую плотность при длинах волн 238 и 316 нм.
Массовые доли (W(ЛС), %) метронидазола и тизоля геля в модельной смеси рассчитывали по формуле (3):
W(ЛС)=(С(ЛС)·М(ЛС)·V(общ)·V2·100)/(102·a·V1·b) (3)
Где, С(ЛС) – молярная концентрация лекарственного средства, моль/л; М(ЛС) – молярная масса (метронидазол 171,15 г/моль, тизоль 2053,79 г/моль); V(общ) – объем хлористоводородной кислоты, необходимый для растворения навески, мл; V1 – объем смеси, отобранный из V(общ), мл; V2 – объем колбы, в которую переносят аликвоту, мл; a – точная навеска, взятая на анализ, г; b – масса лекарственного средства в модельной смеси, г.
При анализе метронидазола и тизоля геля в мази «Метронидазоль», точную навеску мази (около 0,1 г) растворяли в 50,0 мл 0,1 моль/л хлористоводородной кислоты. Далее к 1,5 мл полученного раствора прибавляли ацетатный буферный раствор (рН = 4) до общего объёма 10,0 мл и измеряли оптическую плотность при длинах волн 238 и 316 нм.
Содержание (m(ЛС), г) метронидазола и тизоля геля в мягкой лекарственной форме рассчитывали по формуле (4):
m(ЛС)=(С(ЛС)·М(ЛС)·V(общ)·V2)/(102·a·V1) (4)
Где, С(ЛС) – молярная концентрация лекарственного средства, моль/л; М(ЛС) – молярная масса (метронидазол 171,15 г/моль, тизоль 2053,79 г/моль); V(общ) – объем хлористоводородной кислоты, необходимый для растворения навески, мл; V1 – объем смеси, отобранный из V(общ), мл; V2 – объем колбы, в которую переносят аликвоту, мл; a – точная навеска, взятая на анализ, г.
Установленное содержание тизоля геля в мази (m(ЛС), г) пересчитывали на массовую долю титана (W(Ti), %) по формуле (5):
W(Ti)=(m(ЛС)·2,36%)/10 (5)
Результаты и их обсуждение
С целью разработки способа количественного определения тизоля геля и метронидазола в мази «Метронидазоль» изучены УФ-спектры поглощения в ацетатных буферных растворах при различных значениях pH среды.
Как показали экспериментальные данные, поглощение тизоля геля и метронидазола зависит от состава буферного раствора [5]. Поэтому нами изучены УФ-спектры действующих компонентов в ацетатных буферных растворах при рН = 2–5 (рис. 1).
Рис. 1. УФ-спектры поглощения тизоля геля (А) и метронидазола (В) в ацетатных буферных растворах (концентрация действующих компонентов 8·10-5 моль/л): 1 – рН = 2; 2 – рН = 3; 3 – рН = 4; 4 – рН = 5.
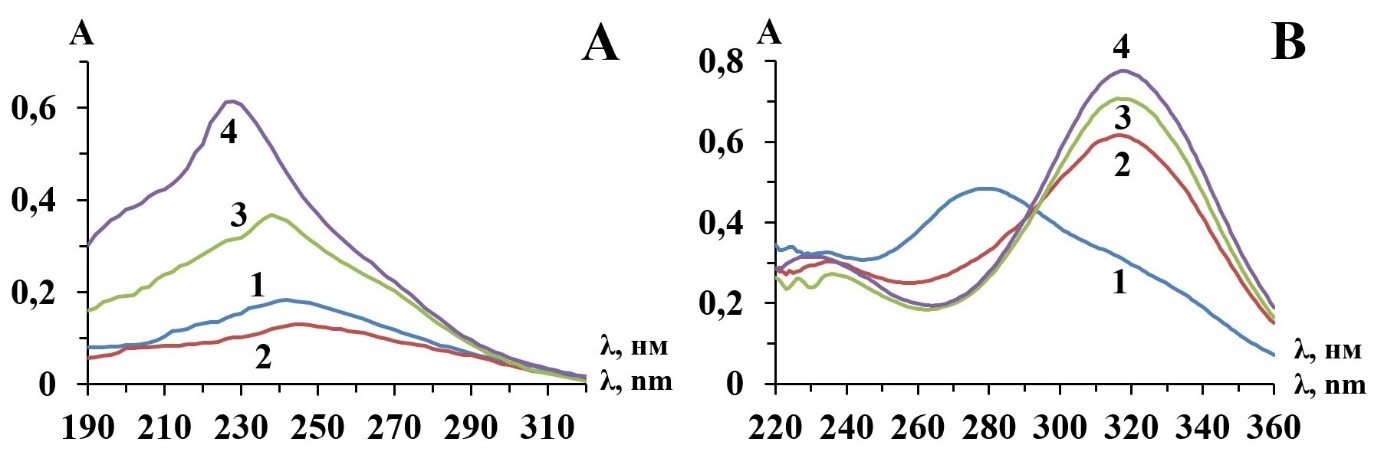
Спектры поглощения растворов тизоля геля в ацетатных буферных растворах с рН = 2 и рН = 3 (рис. 1, А, кривые 1 и 2) характеризуются максимумами при 242 нм (e = 2286,25) и 246 нм (e = 1626,25). УФ-спектры лекарственного средства с рН = 3 и рН = 4 содержат экстремумы при длинах волн 238 нм (e = 4602,50) и 228 нм (e = 7672,50), для которых наблюдается гипсохромное смещение с гиперхромным эффектом на 4 нм и 12 нм соответственно.
Спектральная линия метронидазола в ацетатном буферном растворе с рН = 2 (рис. 1, В, кривая 1) имеет один максимум при длине волны 278–279 нм (e = 6048,75), а также один размытый минимум при 228–230 нм (e = 4010,00–4012,50). Максимумы поглощения метронидазола в буферных растворах с рН = 3 и рН = 4 находятся при длинах волн 316–317 нм (e = 7706,25 и e = 8835,00), а с рН = 5 при 317–318 нм (e = 12087,50). Указанные экстремумы смещены батохромно на 37–38 нм с гиперхромным эффектом относительно максимума поглощения раствора лекарственного средства с рН = 2 (рис.1, В, кривые 2–4). Кроме того, спектральные линии метронидазола в ацетатных буферных растворах характеризуются наличием минимумов при 257–259 нм (e = 3128,75, рН = 3) и 262–264 нм (e = 2302,50, рН = 4, pH = 5) соответственно.
Спектрофотометрическим методом изучена стабильность растворов тизоль геля и метронидазола в ацетатных буферных растворах при различных значениях рН среды. Опыты проводили в ультрафиолетовой области спектра при максимумах светопоглощения. Изменение оптических плотностей растворов лекарственных средств наблюдали во времени на протяжении 60 мин (рис. 2).
Рис. 2. Кривые зависимости оптической плотности растворов тизоля геля (А) и метронидазола (В) от времени в ацетатных буферных растворах (концентрация действующих компонентов 8‧10-5 моль/л): А) 1 – рН = 2, λ = 242 нм; 2 – рН = 3, λ = 246 нм; 3 – рН = 4, λ = 238 нм; 4 – рН = 5, λ = 228 нм; В) 3 – рН = 4, λ = 316 нм; 4 – рН = 5, λ = 318 нм.
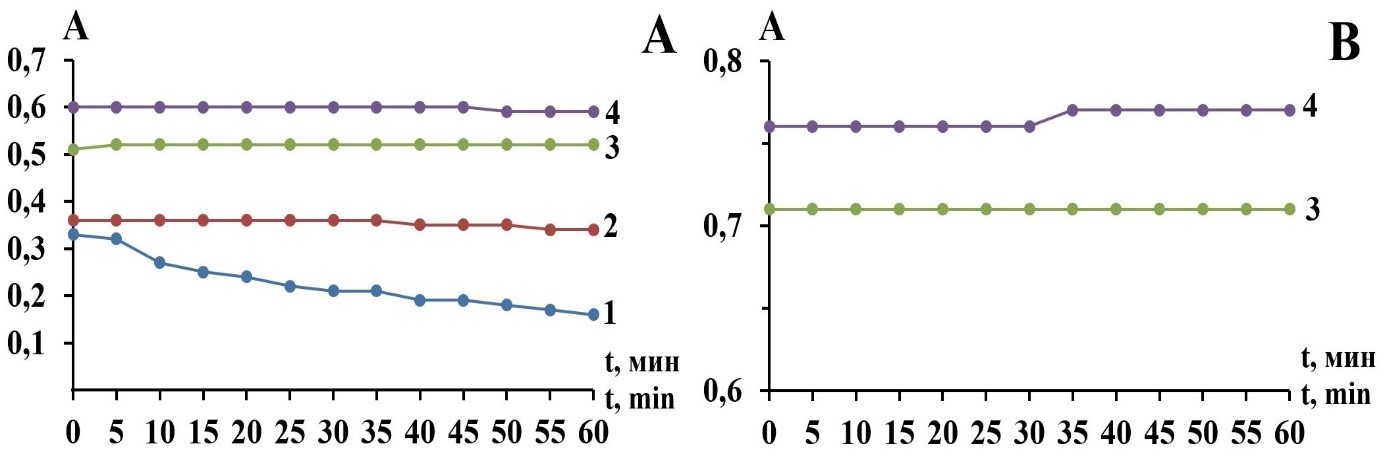
Как показали исследования, раствор тизоля геля в ацетатном буфере с рН = 2 нестабилен во времени. Его оптическая плотность уменьшается в пределах опыта в 2 раза. При рН = 3 раствор лекарственного средства стабилен всего 30 мин. С увеличением рН буферного раствора до 4 и 5 оптическая плотность растворов не изменяется на протяжении 60 мин (рис. 2, А, кривые 3 и 4). Растворы метронидазола отличаются стабильностью в течение опыта (рис. 2, В, кривые 3 и 4). Поэтому для тизоля геля и метронидазола рационально проводить количественный анализ в ацетатных буферных растворах со значениями рН среды 4 и 5. Данные величины водородного показателя буферных растворов будут обеспечивать высокую чувствительность анализа исследуемых компонентов в мази.
Для разработки способа количественного определения двух компонентов в мази «Метронидазоль» исследовали УФ-спектры растворов тизоля геля, метронидазола, их смеси в ацетатном буферном растворе с рН = 4 (рис. 3).
Рис. 3. УФ-спектры поглощения лекарственных средств в ацетатном буферном растворе (рН = 4): 1. Метронидазол (концентрация 8·10-5 моль/л); 2. Тизоль гель (концентрация 1·10-4 моль/л); 3. Смесь метронидазола (концентрация 1·10-4 моль/л) с тизоль гелем (концентрация 1·10-4 моль/л).
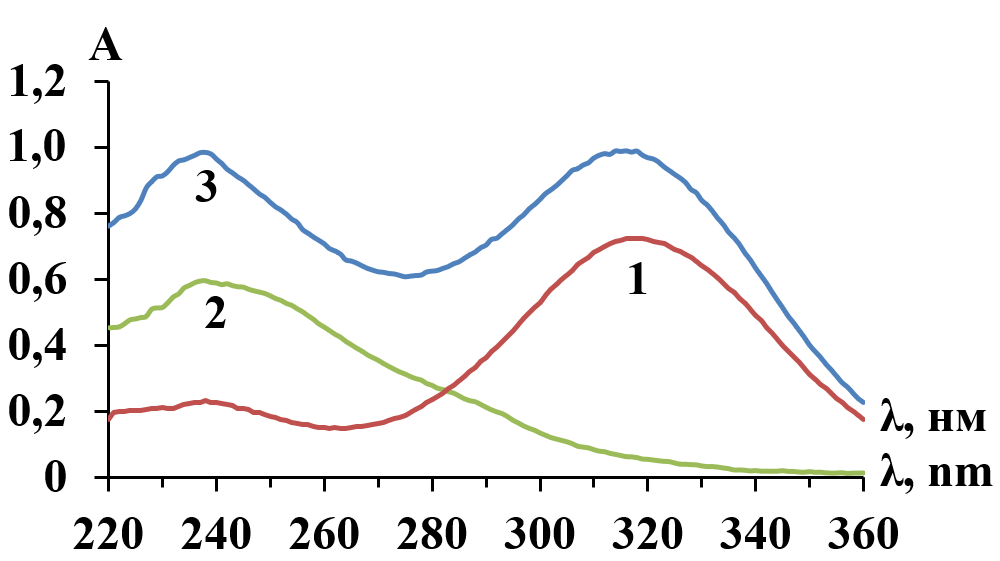
Установлено, что спектральные линии тизоля геля и метронидазола, полученные в ацетатном буферном растворе, перекрываются, а совместные оптические плотности обладают свойством аддитивности (рис. 3, кривая 3). Поэтому для разработки способа оценки количественного содержания лекарственных средств нами выбран метод многоволновой спектрофотометрии. Для определения оптимальных длин волн при анализе исследуемых компонентов в смеси спектрофотометрическим методом рассчитали молярные коэффициенты экстинкции и построили кривую ε(метронидазол) – ε(тизоль) = f(λ) (рис. 4).
Рис. 4. Кривая зависимости разности молярных коэффициентов экстинкции метронидазола и тизоля геля от длины волны
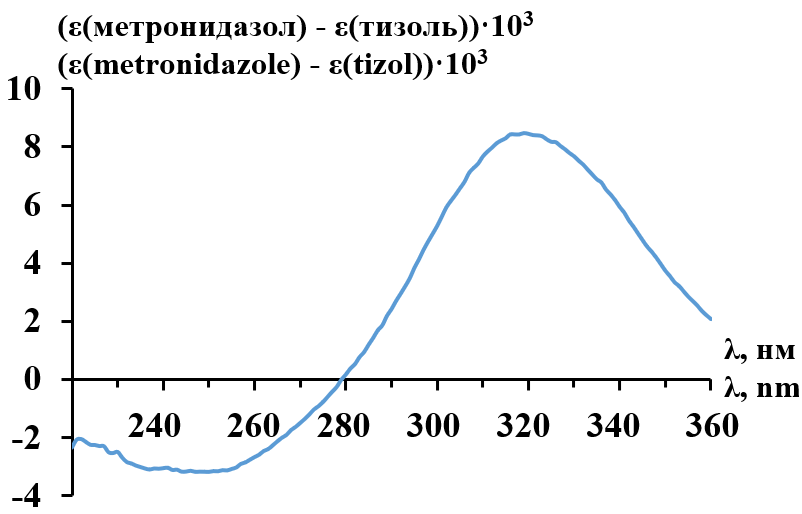
На исследуемой кривой имеется минимум при 238 нм, отвечающий максимуму поглощения тизоля геля [5], и резко выраженный максимум при длине волны 319 нм, который находится вблизи второго экстремума метронидазола (316 нм). Поэтому для количественного спектрофотометрического анализа тизоля геля и метронидазола в смеси целесообразно использовать длины волн 238 нм и 316 нм. Для выполнения расчетов содержания компонентов в мази были установлены молярные коэффициенты экстинкции при аналитических длинах волн (табл. 1).
Таблица 1. Данные расчета молярных коэффициентов экстинкции для тизоля и метронидазола.
| Компоненты мази | С, моль/л | А(238 нм) | ε(238 нм) | А(316 нм) | ε(316 нм) |
|---|---|---|---|---|---|
| Тизоль гель | 0,0001 | 0,596 | 5960,00 | 0,061 | 610,00 |
| Метронидазол | 0,00008 | 0,231 | 2887,50 | 0,724 | 9050,00 |
Для разработки методики количественного анализа метронидазола и тизоля геля в мази «Метронидазоль» применяли модельную смесь с точным содержанием действующих компонентов. Метрологические параметры количественного определения лекарственных средств в модельной смеси оценивали на основании статистической обработки результатов шести параллельных опытов (табл. 2).
Таблица 2. Метрологические параметры количественного определения тизоля геля и метронидазола в модельной смеси.
| Тизоль гель | Метронидазол | ||
|---|---|---|---|
| Найденное содержание | |||
| С1, моль/л | W, % | C2, моль/л | W, % |
| 1,44 · 10-4 1,46 · 10-4 1,44 · 10-4 1,49 · 10-4 1,50 · 10-4 1,54 · 10-4 | 103,43 104,69 102,95 106,18 107,24 109,85 | 8,64 · 10-5 8,79 · 10-5 9,05 · 10-5 9,03 · 10-5 8,93 · 10-5 9,19 · 10-5 | 98,00 99,74 102,68 102,24 101,12 103,97 |
| Среднее значение выборки (W , %) | |||
| 105,72 | 101,29 | ||
| Стандартное отклонение (SD) | |||
| 2,590 | 2,160 | ||
| Стандартное отклонение среднего результата (SW ) | |||
| 1,057 | 0,882 | ||
| Относительное стандартное отклонение среднего результата (RSD, %) | |||
| 2,45 | 2,13 | ||
| Относительная погрешность среднего результата (e , %) | |||
| 2,57 | 2,24 | ||
| Доверительный интервал, % | |||
| 105,72 ± 2,72 (103,00–108,44) | 101,29 ± 2,27 (99,02–103,56) | ||
Рассчитанные величины RSD не превышают 5,00%, относительной погрешности – не превышают 3,00%, что свидетельствует о применимости метода многоволновой спектрофотометрии для количественного анализа тизоля геля и метронидазола в смеси.
Проведенные исследования позволили разработать методику оценки количественного содержания тизоля геля и метронидазола в лекарственном препарате «Метронидазоль» с применением метода многоволновой спектрофотометрии. В табл. 3 представлены результаты количественного спектрофотометрического анализа действующих компонентов в мягкой лекарственной форме.
Таблица 3. Данные анализа тизоля геля и метронидазола в лекарственном препарате «Метронидазоль».
| Тизоль гель | Метронидазол | |||
|---|---|---|---|---|
| C1, моль/л | m(ЛС), г | W(Ti), % | C2, моль/л | m(ЛС), г |
| 1,44 · 10-4 | 9,8254 | 2,32 | 8,64 · 10-5 | 0,4900 |
| 1,46 · 10-4 | 9,9483 | 2,35 | 9,20 · 10-5 | 0,5219 |
| 1,45 · 10-4 | 9,8960 | 2,34 | 8,88 · 10-5 | 0,5034 |
| 1,51 · 10-4 | 10,2381 | 2,42 | 9,13 · 10-5 | 0,5166 |
| 1,48 · 10-4 | 10,0416 | 2,37 | 9,14 · 10-5 | 0,5171 |
| 1,54 · 10-4 | 10,4356 | 2,46 | 9,19 · 10-5 | 0,5199 |
В соответствии с полученными данными, содержание тизоля геля в мази (в пересчете на массовую долю титана) имеет значения 2,32-2,46%, которые входят в допустимые пределы (от 2,23% до 2,48%), установленные в ФСП 42-3157-06. Масса метронидазола в лекарственном препарате составляет 0,4900-0,5219 г при норме отклонений 0,4500-0,5500 г, утвержденной в ОФС.1.8.0001 «Лекарственные препараты аптечного изготовления» [1].
Заключение
Впервые предложено проводить количественный анализ тизоля геля в комплексных лекарственных препаратах. Экспериментально подтверждена возможность применения метода многоволновой спектрофотометрии при количественном анализе тизоля геля и метронидазола в новом лекарственном препарате «Метронидазоль». Разработанная аналитическая методика позволяет определять содержание тизоля геля и метронидазола в мази с относительными погрешностями среднего результата ± 2,72% и ± 2,27% соответственно. Данный способ может быть предложен для введения в документацию по стандартизации и контролю качества новой мягкой лекарственной формы «Метронидазоль».
Список литературы
1. Государственная фармакопея Российской Федерации. XV издание. [Электронный ресурс]. Режим доступа: https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15. (дата обращения 06.06.2024).
2. Еловикова Т.М., Григорьев С.С., Саблина С.Н., Ермишина Е.Ю. Традиции и инновации пародонтологии: аквакомплекс глицеросольвата титана. Екатеринбург: Уральский государственный медицинский университет, 2023. 200 с.
3. Замараева А.И. Перспективы использования спектрофотометрии и химических методов в анализе и изучении свойств новых мягких лекарственных форм, изготовленных на глицерогидрогеле «Тизоль». Вопросы биологической, медицинской и фармацевтической химии 2022; 25(9): 26-33.
4. Кобелева Т.А., Сичко А.И., Замараева А.И., Бессонова Н.С. Разработка способа анализа офлоксацина в комплексном препарате «Офлоксазоль». Разработка и регистрация лекарственных средств. 2021; 10(3): 70-75.
5. Кобелева Т.А., Сичко А.И., Копылова А.И., Попова М.И., авторы; ФГБОУ ВО «Тюменский государственный медицинский университет» Министерства Здравоохранения Российской Федерации, патентообладатель. Способ количественного определения лекарственного препарата Тизоль® геля. Российская Федерация патент RU 2812613 С1. – № 2023117934. 30 января 2024.
6. Копылова А.И., Попова М.И., Кобелева Т.А., Сичко А.И., Емельянов А.А. Использование современных трансдермальных проводников в изготовлении мягких лекарственных форм. Вопросы обеспечения качества лекарственных средств 2023; 1(39): 51-60.
7. Краснюк И.И. (мл.), Нарышкин С.Р., Беляцкая А.В., Тарасов В.В., Степанова О.И., Краснюк И.И., Грих В.В., Овсянникова Л.В., Мазяркин Е.В., Воробьёв А.Н. Метронидазол – 60 лет применения. Вестник Воронежского государственного университета. Серия: Химия. Биология. Фармация 2020; 1: 81-90.
The Use of the Method of Multiwave Spectrophotometry in Quality Control of Tizol Gel and Metronidazole in a New Mild Dosage Form «Metronidazole»
Authors
Kopylova A. I.
Ph.D. (Pharmacy), Assistant, Chair for Chemistry and Pharmacognosy1
Kobeleva T. A.
Doctor of Pharmacy, Professor, Head, Chair for Chemistry and Pharmacognosy1
Sichko A. I.
Doctor of Pharmacy, Professor, Professor, Chair for Chemistry and Pharmacognosy1
1Tyumen State Medical University, Tyumen, Russian Federation
Corresponding Author
Kopylova Anna; e-mail: KopylovaAI@tyumsmu.ru.
Funding
The study had no sponsorship.
Conflict of interest
None declared.
Abstract
Introduction. For the introduction of new medicines into medical practice, a mandatory stage is quality control, which includes determining the quantitative content of active components using modern methods of pharmaceutical analysis. Tizol gel, included in soft dosage forms, is an independent pharmacologically active agent, therefore it is important to evaluate its content in complex medicinal preparations. Aim. To develop a method for quantitative determination of tizol gel and metronidazole in a new semisolid dosage form «Metronidazole» using multiple-wavelength spectrophotometry. Materials and methods. Pharmaceutical substance metronidazole, tizol gel, «Metronidazole» ointment containing 5% nitroimidazole in a tizol base was used for analysis. The studies were performed on spectrophotometer SF-2000 by multiple-wavelength spectrophotometry in the UV region. On the basis of experimental data, the metrological parameters of the developed analytical technique were calculated. Results and discussion. Experimental studies allowed us to justify the use of an acetate buffer solution with pH = 4 as the optimum solvent for the spectrophotometric analysis of tisol gel and metronidazole in the mixture. Analytical wavelengths (238 nm for tisol gel, 316 nm for metronidazole) were selected according to the UV spectra of the drugs obtained. According to the results of quantitative determination of the components of the Metronidazole ointment, the content of medicines is within the limits: metronidazole from 0.4900 to 0.5219 g, tizol gel (in terms of the mass fraction of titanium) – 2.32–2.46%, which are acceptable according to regulatory documentation (FSF 42-3157-06, OFS.1.8.0001). Conclusion. Quantitative analysis of tisol gel in complex pharmaceutical preparations was proposed for the first time. The method of quantitative determination by multiple-wavelength spectrophotometry has been developed which allows to determine the content of tizol gel and metronidazole in a new semisolid dosage form «Metronidazole» with relative errors of the average result not exceeding ± 3.00%.
Key words
metronidazole, tizol gel, multiwave spectrophotometry, quantitative determination
DOI
References
1. Gosudarstvennaja farmakopeja Rossijskoj Federacii. XV izdanie. [The State Pharmacopoeia of the Russian Federation 15th edition]. Available at: https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15. Accessed: 06.06.2024. (In Russ.)
2. Elovikova T.M., Grigor'ev S.S., Sablina S.N., Ermishina E.Ju. Tradicii i innovacii parodontologii: akvakompleks glicerosol'vata titana. [The use of the drug tizol in periodontology, medicine and pharmacy, manual prescriptions of a mild dosage form based on it]. Ekaterinburg: Ural'skij gosudarstvennyj medicinskij universitet, 2023. 200 s. (In Russ.)
3. Zamaraeva A.I. Perspektivy ispol'zovanija spektrofotometrii i himicheskih metodov v analize i izuchenii svojstv novyh mjagkih lekarstvennyh form, izgotovlennyh na glicerogidrogele «Tizol'». [The use of spectrophotometry and chemical methods in the analysis and study of the properties of new soft dosage forms made with Tizol gel]. Voprosy biologicheskoj, medicinskoj i farmacevticheskoj himii [Issues of biological, medical and pharmaceutical chemistry] 2022; 25 (9): 26-33. (In Russ.)
4. Kobeleva T.A., Sichko A.I., Zamaraeva A.I., Bessonova N.S. Razrabotka sposoba analiza ofloksacina v kompleksnom preparate «Ofloksazol'». [Development of a method for the analysis of ofloxacin in the complex preparation «Ofloxazole»]. Razrabotka i registracija lekarstvennyh sredstv [Development and registration of medicines] 2021; 10(3): 70-75. (In Russ.)
5. Kobeleva T.A., Sichko A.I., Kopylova A.I., Popova M.I., inventors; FGBOU VO «Tjumenskij gosudarstvennyj medicinskij universitet» Ministerstva Zdravoohranenija Rossijskoj Federacii, patentoobladatel'. Sposob kolichestvennogo opredelenija lekarstvennogo preparata Tizol'® gelja. [The method of quantitative determination of the drug Tizol® gel]. Russian Federation patent RU 2812613 S1. – № 2023117934. 30 Jan 2024. (In Russ.)
6. Kopylova A.I., Popova M.I., Kobeleva T.A., Sichko A.I., Emel'janov A.A. Ispol'zovanie sovremennyh transdermal'nyh provodnikov v izgotovlenii mjagkih lekarstvennyh form. [The use of modern transdermal conductors in the manufacture of soft dosage forms]. Voprosy obespechenija kachestva lekarstvennyh sredstv [Journal of pharmaceuticals quality assurance issue] 2023; 1(39): 51-60. (In Russ.)
7. Krasnjuk I.I. (ml.), Naryshkin S.R., Beljackaja A.V., Tarasov V.V., Stepanova O.I., Krasnjuk I.I., Grih V.V., Ovsjannikova L.V., Mazjarkin E.V., Vorob'jov A.N. Metronidazol – 60 let primenenija. [Metronidazole – 60 years of use]. Vestnik Voronezhskogo gosudarstvennogo universiteta. Serija: Himija. Biologija. Farmacija [Bulletin of the Voronezh State University. Series: Chemistry. Biology. Pharmacy] 2020; 1: 81-90. (In Russ.)